题目内容
3.下列说法正确的一组是( )①不溶于水的盐(CaCO3、BaSO4等)都是电解质
②酸、碱、盐都是强电解质
③0.5mol•L-1 所有一元酸中氢离子浓度都是0.5mol•L-1
④电解质在通电情况下才能发生电离
⑤电解质溶液导电的原因是在溶液中有自由移动的阴阳离子
⑥熔融的电解质都能导电.
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑤⑥ |
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等.
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物等.
强电解质:水溶液中能完全电离的电解质;
弱电解质:水溶液中只能部分电离的电解质;
物质导电的条件:存在自由电子或者自由移动的离子.
解答 解:①氯化亚汞不溶于水,不是电解质,故错误;
②弱酸、弱碱属于弱电解质,故错误;
③.5mol•L-1 一元强酸中氢离子浓度都是0.5mol•L-1,一元弱酸中氢离子浓度小于0.5mol•L-1,故错误;
④电解质电离不需要,在水溶液中或者熔融状态下就能电离,故错误;
⑤电解质溶液导电的原因是在溶液中有自由移动的阴阳离子,故正确;
⑥熔融的电解质硫酸不导电,故错误;
故选:D.
点评 本题考查了电解质、非电解质、强电解质、弱电解质判断,溶液导电性判断,熟悉电解质、非电解质、强电解质、弱电解质的概念及物质类别是解题关键,注意单质、混合物既不是电解质也不是非电解质,题目难度不大.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
14.用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是( )
| A. | 干燥的 | B. | 不漏水的 | ||
| C. | 用欲配制的溶液润洗过的 | D. | 标有刻度的 |
11.下列操作不能达成实验目的是( )
| A. | 溴乙烷与氢氧化钠溶液共煮后,加入硝酸银检验Br- | |
| B. | 用电石和饱和食盐水制取乙炔 | |
| C. | 用苯、12mol/L的硝酸和18mol/L的硫酸制硝基苯 | |
| D. | 用稀硝酸洗涤做过银镜反应的试管 |
18.下列有关离子的检验,正确的是( )
| A. | 某化合物焰色反应呈黄色,说明该物质中一定含有Na+ | |
| B. | 向某溶液中加入盐酸有气泡产生,说明一定有CO32- | |
| C. | 向某溶液中加入氯化钡溶液,有白色沉淀产生,说明一定有SO42- | |
| D. | 向某溶液中加入硝酸银溶液,有白色沉淀产生,说明一定有Cl- |
15.汽车尾气处理装置中发生如下反应,2NO+2CO═N2+2CO2,下列说法正确的是( )
| A. | NO是氧化剂 | B. | CO发生还原反应 | ||
| C. | NO失去电子 | D. | 该反应是复分解反应 |
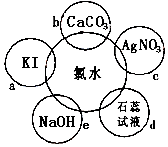 (1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量): .
.