题目内容
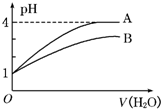 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )| A、A酸比B酸的电离程度小 |
| B、pH=1时,B酸的物质的量浓度比A酸大 |
| C、B酸比A酸容易电离 |
| D、A是强碱,B是弱碱 |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:pH均为1酸,如果酸是强酸,稀释1000倍后,溶液的pH应该为4,如果是弱酸,因为存在电离平衡,导致稀释后的溶液中氢离子大于原来的千分之一,则溶液的pH应该大于1小于4,根据图象知,溶液稀释后,A的pH为4,B的小于4,所以A是强酸,B是弱酸.
解答:
解:pH均为1酸,如果酸是强酸,稀释1000倍后,溶液的pH应该为4,如果是弱酸,因为存在电离平衡,导致稀释后的溶液中氢离子大于原来的千分之一,则溶液的pH应该大于1小于4,根据图象知,溶液稀释后,A的pH为4,B的小于4,所以A是强酸,B是弱酸,
A.A是强酸完全电离,B是弱酸,部分电离,所以A酸比B酸的电离程度大,故A错误;
B.A是强酸,B是弱酸,所以B中存在电离平衡,当pH相等时,弱酸的物质的量浓度大于强酸,故B正确;
C.A是强酸,B是弱酸,所以A比B容易电离,故C错误;
D.通过以上分析知,A是强酸,B是弱酸,故D错误;
故选B.
A.A是强酸完全电离,B是弱酸,部分电离,所以A酸比B酸的电离程度大,故A错误;
B.A是强酸,B是弱酸,所以B中存在电离平衡,当pH相等时,弱酸的物质的量浓度大于强酸,故B正确;
C.A是强酸,B是弱酸,所以A比B容易电离,故C错误;
D.通过以上分析知,A是强酸,B是弱酸,故D错误;
故选B.
点评:本题考查强弱电解质溶液稀释时的pH的浓度变化,注意加水促进弱酸电离,所以弱酸PH变化慢,题目难度较小.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
在一定温度下,反应AB(g)?
A2(g)+
B2(g)的平衡常数为0.1.若将1.0mol的AB(g)通入体积为1.0L的密闭容器中,在该温度时AB(g)的最大分解率接近于( )
| 1 |
| 2 |
| 1 |
| 2 |
| A、5% | B、17% |
| C、25% | D、33% |
以下分离混合物的操作中,不正确的是( )
A、蒸发时,蒸发皿内所盛液体不超过蒸发皿容积的
| ||
| B、蒸发结晶时,不能直接蒸干液体,最后少量液体用余热蒸干 | ||
| C、用四氯化碳萃取碘水中的碘,分液时四氯化碳碘溶液从上口倒出 | ||
| D、蒸馏时,要在烧瓶中加入几粒碎瓷片 |
要想使AlCl3溶液中的Al3+全部沉淀下来,应选用下列试剂中的( )
| A、石灰水 | B、氢氧化钠溶液 |
| C、硫酸 | D、氨水 |
关于实验室中的下列叙述,正确的是( )
| A、金属钠着火燃烧时,用泡沫灭火器灭火 |
| B、硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 |
| C、在新制氯水中滴加少量紫色石蕊试液,充分振荡后溶液最终呈红色 |
| D、向Ba(OH)2溶液中慢慢滴加稀硫酸至过量,溶液的导电性变化是弱→强→弱 |
某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品是( )
| A、乙二醇(C2H6O2) |
| B、乙醇 |
| C、乙醛 |
| D、甲烷和丙烷(C3H8)的混合物 |
在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是( )
| A、滤液中一定有Fe(NO3)3 |
| B、滤渣只含Ag和Cu,一定无Zn |
| C、滤渣中一定有Ag、Cu和Fe,一定无Zn |
| D、滤渣中可能有Ag、Cu、Fe和Zn |
 分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )