题目内容
20.某研究小组研究了其他条件不变时,改变条件对以下可逆反应的影响:2SO2(g)+O2(g)?2SO3(g)+Q下列说法正确的是( )| A. |  研究的是温度、压强对平衡的影响,横坐标表示压强 | |
| B. | 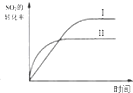 研究的是温度对平衡的影响,Ⅱ采用的温度更高 | |
| C. |  图中t0时使用了催化剂,使平衡向正反应方向进行 | |
| D. | 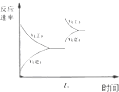 图中t0时增大压强,使平衡向正反应方向进行 |
分析 根据影响化学反应速率和化学平衡的因素进行判断得出正确结论.升高温度,化学反应速率加快,平衡向着吸热的方向移动;增大压强,化学反应速率加快,平衡向着气体体积减小的方向移动;使用催化剂,加快化学反应速率,对平衡不产生影响.
解答 解:A.横坐标表示压强,升高温度,平衡逆向移动,SO2转化率减小,与图象不符,横坐标应为温度,故A错误;
B.升高温度,加快化学反应速率,平衡逆向移动,与图象相符,故B正确;
C.使用催化剂,加快化学反应速率,对平衡不产生影响,故C错误;
D.增大压强,正逆反应速率瞬时增大,平衡正向移动,正反应速率大于逆反应速率,故D正确,
故选BD.
点评 本题考查外界条件对化学反应速率和化学平衡的影响,题目难度中等.要注意催化剂对化学平衡无影响.

练习册系列答案
相关题目
1.4-甲基-2-戊炔分子中在同一直线上的碳原子数为( )
| A. | 5个 | B. | 4个 | C. | 3个 | D. | 2个 |
11.X、Y、Z和R分别代表四种元素,如果aXm+、bYn+、cZn-、dRm-四种离子的电子层结构相同(a、b、c、d为元素的核电荷数),则下列关系正确的是( )
| A. | a-c=m-n | B. | a-b=n-m | C. | c-d=m+n | D. | b-d=m+n |
8.钾长石的主要成分为硅酸盐,由前20号元素中的四种组成,化学式为XYZ3W8.其中,只有W显负价.X、Y的最外层电子数之和与Z的最高正价数相等.Y3+与W的阴离子具有相同的电子层结构.X、W的质子数之和等于Y、Z的质子数之和.下列说法错误的是( )
| A. | W的离子半径>Y的离子半径 | |
| B. | Z的氢化物稳定性<W的氢化物稳定性 | |
| C. | Y的氧化物既能与盐酸,又能与NaOH溶液反应 | |
| D. | X2W2、Y2W3两种化合物含有的化学键类型完全相同 |
9.下列说法中正确的是(NA为阿伏加德罗常数的值)( )
| A. | 1mol苯分子中所含的C=C键数为3NA | |
| B. | 60gSiO2中含有Si-O键的个数为2NA | |
| C. | 0.1molCnH2n+2中含有的碳碳单键数为0.1nNA | |
| D. | 18 g冰中含氢键的个数为2NA |
10.关于苯,下列说法正确的是( )
| A. | 苯不溶于水,密度比水大 | |
| B. | 苯不能发生氧化反应 | |
| C. | 除去苯中混有的少量甲苯,可以用酸性高锰酸钾溶液 | |
| D. | 苯可以跟溴水反应制取溴苯 |
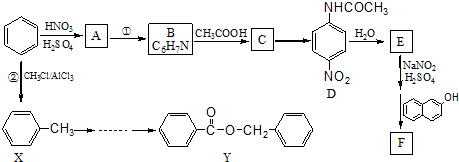
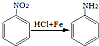
 .
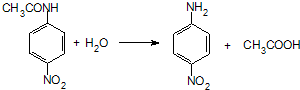
.
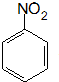 、F
、F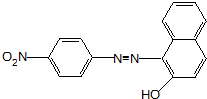 .
.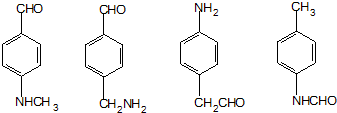 (其中两种)
(其中两种)  .
.

 ;F
;F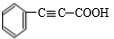 .
. +
+ $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$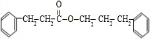 +H2O.
+H2O.