题目内容
9.下列对如图两烧杯溶液分析一定正确的是( )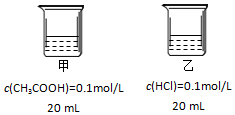
| A. | 甲、乙两烧杯中水电离出的H+浓度:甲<乙 | |
| B. | 分别稀释相同倍数,溶液pH变化:甲=乙 | |
| C. | 相同条件下,AgCl(s)在甲中溶解度大于在乙中 | |
| D. | 向甲烧杯加入NaOH使溶液中性后一定存在:c(Na+)=c(CH3COO-)+c(CH3COOH) |
分析 A.溶液的酸性越强,则对水的电离抑制程度越大;
B.加水稀释,弱电解质的电离平衡被促进;
C.乙中含有的氯离子对AgCl的溶解平衡有抑制作用;
D.根据电荷守恒判断.
解答 解:A.溶液的酸性越强,则对水的电离抑制得越厉害,由于乙烧杯中含有强电解质HCl,故乙烧杯中的酸性比甲强,则对水的电离的抑制更强,即乙中水的电离程度更小,水电离出H+浓度:甲>乙,故A错误;
B.加水稀释,弱电解质的电离平衡被促进,故甲中氢离子浓度下降较乙中的慢,则pH变化甲<乙,故B错误;
C.乙中含有的氯离子对AgCl的溶解平衡有抑制作用,故相同条件,AgCl(s)在甲中溶解度大于在乙中,故C正确;
D.向甲烧杯加入NaOH使溶液中性,溶液中存在电荷守恒:c(H+)+c(Na+)=c(CH3COO-)+c(OH-),由于溶液显中性,即c(H+)=c(OH-),所以溶液中c(Na+)=c(CH3COO-),故D错误.
故选C.
点评 本题考查了弱电解质的电离平衡的移动和溶解平衡的移动等问题,综合性较强,难度适中,注意加水稀释对弱电解质的电离平衡的影响,侧重于考查学生的分析能力和应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.煤的气化主要反应是煤中碳与水蒸气反应生成CO、H2等,回答下列问题:
(1)CO和H2分别与O2都可以设计成燃料电池,CO与O2设计成燃料电池(以熔融碳酸盐为电解质)负极的电极反应为CO-2e-+CO32-=2CO2
(2)在煤的气化获得的化工原料气中含有少量羰基硫(COS),能引起催化中毒、大气污染等,COS的电子式为 羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:
羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:
①氢解反应:COS(g)+H2(g)═H2S(g)+CO(g)△H1=+7kJ/mol
②水解反应:COS(g)+H2O(g)═H2S(g)+CO2(g)△H2
已知反应中相关的化学键键能数据如表
则△H2=-35kJ/mol
(3)脱硫处理后的CO和H2在催化剂作用下合成甲醇:CO2(g)+3H 2(g)?CH3OH(g)+H2O(g)△H2=-90.14kJ/mol,该反应能自发的理由是该反应是焓减、熵减反应,低温时自发.
①一定温度下,在两个容积都为VL的恒容密闭容器中,找如下方式反应物,一段时间后达到平衡
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则n的取值范围为0.4<n≤1,反应的平衡常数K=0.046V2.
②甲容器保持恒容,欲增大H2的平衡转化率,可采取的措施有增大CO的投入量、分离出甲醇、适当降温(答两点即可).
(1)CO和H2分别与O2都可以设计成燃料电池,CO与O2设计成燃料电池(以熔融碳酸盐为电解质)负极的电极反应为CO-2e-+CO32-=2CO2
(2)在煤的气化获得的化工原料气中含有少量羰基硫(COS),能引起催化中毒、大气污染等,COS的电子式为
 羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:
羰基硫与烧碱溶液反应生成水和两种正盐的离子方程式为COS+4NaOH=Na2S+Na2CO3+2H2O羰基硫的脱硫常用两种方法,其反应式分别为:①氢解反应:COS(g)+H2(g)═H2S(g)+CO(g)△H1=+7kJ/mol
②水解反应:COS(g)+H2O(g)═H2S(g)+CO2(g)△H2
已知反应中相关的化学键键能数据如表
| 化学键 | C=O(CO2) | C=O(COS) | C=S | H-S | H-O |
| 键能(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
(3)脱硫处理后的CO和H2在催化剂作用下合成甲醇:CO2(g)+3H 2(g)?CH3OH(g)+H2O(g)△H2=-90.14kJ/mol,该反应能自发的理由是该反应是焓减、熵减反应,低温时自发.
①一定温度下,在两个容积都为VL的恒容密闭容器中,找如下方式反应物,一段时间后达到平衡
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | mmolCO2、3mmolH2、 nmolCH3OH(g)、nmolH2O(g) |
②甲容器保持恒容,欲增大H2的平衡转化率,可采取的措施有增大CO的投入量、分离出甲醇、适当降温(答两点即可).
13.下列容器不能用来盛放冷的浓硫酸和浓硝酸的是( )
| A. | 铁制容器 | B. | 铝制容器 | C. | 铜制容器 | D. | 玻璃容器 |
17.由分类思想,下列说法正确的是( )
| A. | 氢氧化钠、盐酸都为强电解质 | |
| B. | 铁生锈、食物腐败都有氧化反应发生 | |
| C. | 糖类、蛋白质都为高分子化合物 | |
| D. | 一氧化碳和二氧化碳都是酸性氧化物 |
14.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、I-、SCN- | |
| C. | pH=13的溶液中:K+、NH4+、SO42-、NO3- | |
| D. | 由水电离产生的c(OH-)=1×10-12mol•L-1的溶液中:K+、Na+、Cl-、NO3- |
1.有9种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚乙炔;⑧环己烯;⑨聚氯乙烯,其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A. | ①②③⑤ | B. | ①④⑥⑧ | C. | ①④⑥⑨ | D. | ①④⑤⑦ |
18.MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为:
(1)软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O
(2)除去反应混合物中的不溶物
(3)电解混合液MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4
下列说法不正确的是( )
(1)软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S+2H2O
(2)除去反应混合物中的不溶物
(3)电解混合液MnSO4+ZnSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$MnO2+Zn+2H2SO4
下列说法不正确的是( )
| A. | ①中MnO2和H2SO4都是氧化剂 | B. | 硫酸在该生产中可循环使用 | ||
| C. | ①中析出16gS时转移1mol电子 | D. | ②中MnSO4发生氧化反应 |
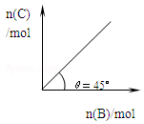 在盛有足量A的体积可变的密闭容器中,保持压强一定,加入B,发生反应:A(s)+2B(g)?4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
在盛有足量A的体积可变的密闭容器中,保持压强一定,加入B,发生反应:A(s)+2B(g)?4C(g)+D(g);△H<0.在一定温度、压强下达到平衡.平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是