题目内容
9.下列实验不用水浴加热的是( )| A. | 实验室制乙烯 | B. | 苯的硝化 | C. | 银镜反应 | D. | 乙酸乙酯的制备 |
分析 因为水的沸点是100℃,用水浴加热,所以“水浴”加热温度不可能超过100℃,水浴加热的温度是使反应容器内试剂受热温度均匀,据此即可解答.
解答 解:A.实验室利用加热到170℃时乙醇和浓硫酸混合溶液制取乙烯,反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,反应的温度为170℃,超过沸水的温度,不能用水浴,故A选;
B.苯和浓硝酸、浓硫酸在50℃~60℃发生硝化反应生成硝基苯和水,该反应为C6H6+HNO3$→_{△}^{浓硫酸}$C6H5NO2+H2O,需要水浴,故B不选;
C.制备银镜时,如葡萄糖发生银镜反应的方程式为:CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH $\stackrel{水浴}{→}$CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O,用酒精灯的外焰银镜反应需要的温度不超过100℃,给试管底部加热时温度太高,应该用水浴加热,故C不选;
D.制取乙酸乙酯需要的温度较高,需要用酒精灯直接加热,不能用水浴加热,故D选;
故选AD.
点评 本题考查了化学实验方案的评价,题目难度不大,明确常见反应原理、反应条件为解答关键,注意掌握水浴加热的要求,试题在注重对基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
20.分枝酸可用于生化研究,其结构简式如图.下列关于分枝酸的叙述正确的是( )
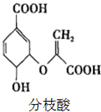

| A. | 分枝酸的分子式为C10H8O6 | |
| B. | 分枝酸能发生取代、加成、氧化反应 | |
| C. | 1mol分枝酸最多可与3molNaOH发生中和反应 | |
| D. | 1mol分枝酸最多可与2molBr2发生反应 |
17.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 在1mol甲基(-CH3)中,电子总数9NA | |
| B. | 在1mol的Na2O2中,有2NA个阴离子 | |
| C. | 标准状况下,22.4L CHC13所含有的分子数目为NA | |
| D. | Cu、A1为电极,浓硝酸为电解质溶液所构成的原电池中,导线上流过NA个电子,则A1电极放出气体的体积一定为22.4L |
14.如图所示高聚物的单体有几种( )
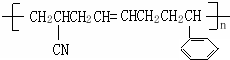
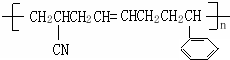
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
1.下列措施对增大反应速率明显有效的是( )
| A. | 在H202分解中加入MnO2 | |
| B. | Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 | |
| C. | 在NaOH与HCL两溶液反应时,增大压强 | |
| D. | Na与水反应时增大水的用量 |
