题目内容
9.25℃时,某一元强碱溶液的pH为a,某一元酸HA溶液的pH为b,电离度为1.0%,若将1体积的此强碱溶液与10体积的HA溶液混合,恰好完全反应,则a与b之和为( )| A. | 14 | B. | 15 | C. | 16 | D. | 17 |
分析 25℃时,某一元强碱溶液的pH为a,则溶液中c(OH-)=10a-14mol/L,某一元酸HA溶液的pH为b,c(H+)=10-bmol/L,电离度为1.0%,则酸为弱酸,其浓度c(HA)=$\frac{1{0}^{-b}mol/L}{1.0%}$=102-bmol/L,然后根据将1体积的此强碱溶液与10体积的HA溶液混合,恰好完全反应来分析.
解答 解:25℃时,某一元强碱溶液的pH为a,则溶液中c(OH-)=10a-14mol/L,某一元酸HA溶液的pH为b,c(H+)=10-bmol/L,电离度为1.0%,则酸为弱酸,其浓度c(HA)=$\frac{1{0}^{-b}mol/L}{1.0%}$=102-bmol/L,而将1体积的此强碱溶液与10体积的HA溶液混合,恰好完全反应,故有:10a-14mol/L×VL=102-bmol/L×10VL
解得a+b=15.
故选B.
点评 本题考查了强碱和弱酸混合后的有关计算,应注意的是电离度=$\frac{物质电离的物质的量}{物质的总物质的量}$×100%,难度不大.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
19.短周期主族元素A、B、C、D的原子序数依次增大.已知A、C的原子序数之差为8,A、B、C三种元素原子的最外层电子数之和为15,B元素原子的最外层电子数等于A元素原子的最外层电子数的一半,下列叙述正确的是( )
| A. | 简单离子的半径:B>C>D>A | |
| B. | 氢化物的稳定性:C>D | |
| C. | B和其他3种元素均能形成离子化合物 | |
| D. | B与D形成的化合物溶于水所得溶液显酸性 |
20.石英与焦炭在高温的氮气流中发生可逆反应,能制得新型陶瓷材料氮化硅(Si3N4):SiO2(s)+C(s)+N2(g)$\stackrel{高温}{→}$Si3N4(s)+CO(g)(未配平)△H<0.下列叙述正确的是( )
| A. | 该反应的氧化剂为N2,还原产物为CO | |
| B. | 反应中每生成0.1mol Si3N4转移电子的物质的量为1.2mol | |
| C. | 增大压强平衡向正反应方向移动 | |
| D. | 反应平衡常数表示为K=$\frac{c(CO)}{c({N}_{2})}$,升高温度K值增大 |
14.第ⅢA族R元素在地壳中的丰度约为0.001%,单质熔点2180℃,原子半径小于铍,则关于R的叙述不正确的是( )
| A. | 是非金属元素 | B. | 单质是分子晶体 | ||
| C. | R(OH)4-结合H+的能力小于Al(OH)4- | D. | R2H6中R为-3价 |
1.研究小组为探究弱酸性条件下铁发生电化学腐类型的影响因素,将2.0g新制铁粉和0.5g碳粉混合均匀并置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
实验测得容器中压强随时间变化如图2,.则下列说法不正确的是( )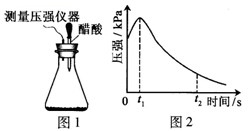
实验测得容器中压强随时间变化如图2,.则下列说法不正确的是( )

| A. | t2时容器中压强明显小于起始压强原因是铁发生了吸氧腐蚀 | |
| B. | 0~t2时压强变大的原因可能是铁发生了析氢腐蚀 | |
| C. | 0~t1时压强变大的原因可能是腐蚀过程为放热反应,锥形瓶内气体温度升高 | |
| D. | 钢铁在酸性条件下一定发生析氢腐蚀 |
8.自从1902年德国化学家哈伯研究出合成氨的方法以来,氮的固定的相关研究获得了不断的发展.
(1)分析下表数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.2260℃时,向2L密闭容器中充入0.3molN2和0.3molO2,模拟大气固氮反应,达到平衡时,N2的转化率是33.3%(结果保留三位有效数字).
(2)工业固氮的主要形式是:N2 (g)+3H2 (g)?2NH3 (g)△H<0,如图是当反应器中按n(N2):n(H2)=1:3 投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线.
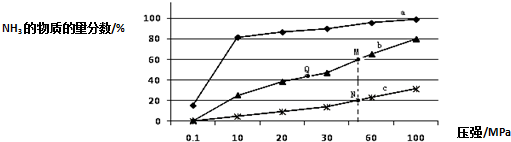
①曲线a对应的温度是200℃.
②关于工业合成氨的反应,下列叙述正确的是A(填字母).
A.图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
B.工业合成氨之所以加入催化剂,是因为加入催化剂有利于提高反应的活化能
C.相同压强下,投料相同,达到平衡所需时间关系为c>b>a
③N点时c(NH3)=0.2mol/L,N点的化学平衡常数K=0.93(结果保留两位小数).
(3)合成氨原料气中的氢气可用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2mol CO2吸收316kJ热量,该反应的热化学方程式是CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+158kJ/mol,该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是CO32-+CO2+H2O=2HCO3-.
(4)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
(1)分析下表数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.2260℃时,向2L密闭容器中充入0.3molN2和0.3molO2,模拟大气固氮反应,达到平衡时,N2的转化率是33.3%(结果保留三位有效数字).
| 反应 | 大气固氮N2(g)+O2(g)?2NO(g) | |
| 温度/℃ | 27 | 2260 |
| K | 3.84×10-31 | 1 |

①曲线a对应的温度是200℃.
②关于工业合成氨的反应,下列叙述正确的是A(填字母).
A.图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
B.工业合成氨之所以加入催化剂,是因为加入催化剂有利于提高反应的活化能
C.相同压强下,投料相同,达到平衡所需时间关系为c>b>a
③N点时c(NH3)=0.2mol/L,N点的化学平衡常数K=0.93(结果保留两位小数).
(3)合成氨原料气中的氢气可用天然气(主要成分为CH4)在高温、催化剂作用下与水蒸气反应制得,反应中每生成2mol CO2吸收316kJ热量,该反应的热化学方程式是CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+158kJ/mol,该方法制得的原料气中主要杂质是CO2,若用K2CO3溶液吸收,该反应的离子方程式是CO32-+CO2+H2O=2HCO3-.
(4)合成氨工业中含氨废水的处理方法之一是电化学氧化法,将含氨的碱性废水通入电解系统后,在阳极上氨被氧化成氮气而脱除,阳极的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
9.下列五种烃:①正丁烷 ②异丁烷 ③丙烷 ④辛烷 ⑤乙烷,按它们的沸点由高到低的顺序排列为( )
| A. | ①④②③⑤ | B. | ④①②③⑤ | C. | ⑤③②①④ | D. | ④①③⑤② |
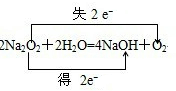
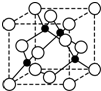 A、B、C、D、E、F是周期表前四周期的元素,且原子序数依次递增,已知A是宇宙中含量最多的元素,B元素能形成的化合物种类最多,E原子的半径是所在周期最大的,E和D形成的某化合物是呼吸面具中气的来源,F基态原子有6个来成对电子.请回答下列问题:
A、B、C、D、E、F是周期表前四周期的元素,且原子序数依次递增,已知A是宇宙中含量最多的元素,B元素能形成的化合物种类最多,E原子的半径是所在周期最大的,E和D形成的某化合物是呼吸面具中气的来源,F基态原子有6个来成对电子.请回答下列问题: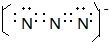 ;
; ;
;