题目内容
5.下列各项试验相应操作、实验现象及原因解释或推论合理的是( )| 选项 | 操作 | 现象 | 解释或理论 |
| A | 把铁片投入浓硫酸 | 无明显变化 | 常温下铁不与浓硫酸反应 |
| B | 将浓硫酸滴到白纸上 | 白纸变黑 | 浓硫酸具有强氧化性,导致纸中的纤维素碳化 |
| C | 把二氧化硫通入溴水 | 溴水褪色 | 说明二氧化硫具有漂白性 |
| D | 用湿润的红色石蕊试纸检验某气体 | 试纸变蓝 | 该气体是氨气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.常温下浓硫酸与铁发生钝化反应;
B.浓硫酸表现脱水性;
C.二氧化硫和溴发生氧化还原反应;
D.氨气的水溶液呈碱性.
解答 解:A.铁片投入浓硫酸,没有明显变化,是由于铁与浓硫酸发生钝化反应,在表面生成一层致密的氧化物膜而阻碍反应的继续进行,并不是不反应,故A错误;
B.浓硫酸具有脱水性,使纤维素碳化,故B错误;
C.二氧化硫与溴水发生氧化还原反应,不是表面的漂白性,故C错误;
D.试纸变蓝,说明气体水溶液呈碱性,溶液呈碱性的气体只有氨气,故D正确.
故选D.
点评 本题考查较为综合,多角度考查元素化合物知识,为高频考点,侧重于学习的分析能力和评价能力的考查,注意把握物质的性质的异同,难度不大.

练习册系列答案
相关题目
15.已知X、Y是主族元素,I为电离能,单位kJ/mol.根据表所列数据判断错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 若元素Y处于第3周期,它可与冷水剧烈反应 | |
| C. | 元素X与氯形成化合物时,化学式可能是XCl | |
| D. | 元素Y是ⅢA族的元素 |
16.在强碱性的无色透明溶液中,能大量共存的离子是( )
| A. | Ca2+,Na+,NO3-,Cl- | B. | K+,Ba2+,Cl-,NO3- | ||
| C. | Na+,HCO3-,CO32-,K+ | D. | Na+,Cl-,K+,MnO4- |
20.鉴别下列各组有机物,所选用的试剂不正确的是( )
| A. | 鉴别苯与四氯化碳:碘水 | |
| B. | 鉴别甲烷与乙烯:酸性高锰酸钾溶液 | |
| C. | 鉴别 与CH≡CH:溴水 与CH≡CH:溴水 | |
| D. | 鉴别NaCl与CH3CH2Cl:硝酸银溶液 |
10.下列离子组能大量共存且加入相应试剂后发生反应的离子方程式正确的是( )
| 离子组 | 加入试剂 | 加入试剂后发生反应 | |
| A | K+、Fe2+、I- | 少量的酸性KMnO4溶液 | 5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O |
| B | Fe3+、I-、SO42- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| C | Ba2+、HCO3-、Cl- | NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| D | Al3+、Cl-、NO3- | 过量浓氨水 | Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
| A. | A | B. | B | C. | C | D. | D |
17.亚硫酸盐在工业生产中冇广泛的应用,某同学在实验中对亚硫酸盐的制备和性质进行探究.
(1)Cu2SO3•CuSO3•2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示.
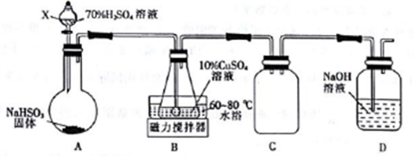
①仪器X的名称是分液漏斗.常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是SO2易溶于水,用较浓的硫酸有利于SO2的逸出.
②装置C的作用是防止倒吸.
③装置B中发生反应的离子方程式为3Cu2++3SO2+6H2O═Cu2SO3•CuSO3•2H2O↓+8H++SO42-.
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是防止Cu2SO3•CuSO3•2H2O发生分解和被氧化.
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量.甲同学欲通过下列实验确定该反应属于哪一种情况,请完成表:
(3)请设计简单实验方案比较室温下NaHSO3浓液中HSO3-的电离平衡常数Ka与水解平衡常数Kb的相对大小:常温下,用pH试纸(或pH计)测定NaHSO3溶液的pH,若PH<7,则Ka>Kb;若pH>7,则Ka<Kb.
(1)Cu2SO3•CuSO3•2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示.

①仪器X的名称是分液漏斗.常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是SO2易溶于水,用较浓的硫酸有利于SO2的逸出.
②装置C的作用是防止倒吸.
③装置B中发生反应的离子方程式为3Cu2++3SO2+6H2O═Cu2SO3•CuSO3•2H2O↓+8H++SO42-.
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是防止Cu2SO3•CuSO3•2H2O发生分解和被氧化.
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量.甲同学欲通过下列实验确定该反应属于哪一种情况,请完成表:
| 实验操作 | 预期现象及结论 |
| 取上述反应后的混合溶液于试管 A中,滴加稀硫酸 | 若有气泡产生,则①II(填“I”“II”或“III”,下同)成立,若没有气泡产生,则②I或III成立 |
| 另取上述反应后的混合溶液于试管B中,滴加几滴淀粉KI溶液,充分振荡 | ③溶液变为蓝色,则III成立 |
14.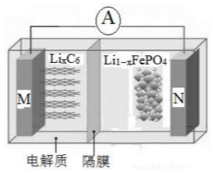 磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图.M电极是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xFeO4$?_{充电}^{放电}$LiFePO4+6C.下列说法正确的是( )
磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图.M电极是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xFeO4$?_{充电}^{放电}$LiFePO4+6C.下列说法正确的是( )
 磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图.M电极是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xFeO4$?_{充电}^{放电}$LiFePO4+6C.下列说法正确的是( )
磷酸铁锂电池具有高效率输出、可快速充电、对环境无污染等优点,其工作原理如图.M电极是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xFeO4$?_{充电}^{放电}$LiFePO4+6C.下列说法正确的是( )| A. | 放电时Li+从右边移向左边 | |
| B. | 放电时M是负极,电极反应式为:C6x--xe-═6C | |
| C. | 充电时电路中通过0.5mol电子,消耗36gC | |
| D. | 充电时N极连接电源的正极,电极反应式为:LiFePO4-xe-═Li1-xFeO4+xLi+ |
15.设NA为阿伏加德罗常数的值,下列物质所含粒子数目为NA的是( )
| A. | 7 g乙烯和丙烯混合气体中的氢原子数目 | |
| B. | 0.5 mol Fe溶于过量HNO3溶液中,转移的电子数目 | |
| C. | 2.5 L 0.4 mol/L 的 Na2CO3 溶液中 CO32-数目 | |
| D. | 标准状况下,5.6 L CCl4含有的共价键数目 |