题目内容
(13分)四氯化硅是粗硅精炼中的中间产物,熔点-70℃,沸点57.6℃,在潮湿空气中水解生成硅酸和氯化氢。某兴趣小组在实验室里通过下图所示装置制取少量四氯化硅: 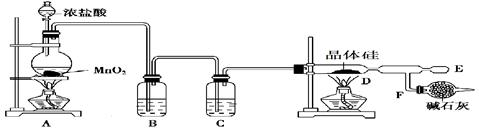
如何检验上图气体发生装置的气密性: ______________________
A装置中发生反应的离子方程式为: ________________________
A装置中玻璃实验仪器名称为(写出两种即可):_______和_______
B中的液体为:______________F中碱石灰的作用为:① __________②________
先加热图中哪个装置:__________________原因:________________________
若实验中用12mol·L-1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量
总是小于0.03mol,试分析可能存在的原因是:① __________② _________
⑴堵住导管出口,打开分液漏斗活塞,向分液漏斗中注入蒸馏水,过一会,如果分液漏斗中液面不再下降,则气密性良好。(其他合理答案也可)(2分)
⑵ MnO2+4H++2Cl-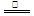 Mn2++Cl2↑+2H2O (2分)
Mn2++Cl2↑+2H2O (2分)
⑶分液漏斗(1分)和圆底烧瓶(1分)(分液漏斗、酒精灯、圆底烧瓶任写两种)
⑷饱和食盐水(1分)①吸收多余氯气(1分)②防止空气中水蒸气从末端进入D中(1分)
⑸A(1分)原因:利用A所产生的氯气排尽装置中的空气等,防止硅与空气反应(1分)
⑹①盐酸挥发(1分)②随着反应进行,浓盐酸会变稀,稀盐酸不和二氧化锰反应(1分)
解析

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
 下列是部分矿物资源的利用及产品流程如图,有关说法不正确的是( )
下列是部分矿物资源的利用及产品流程如图,有关说法不正确的是( )| A、粗铜电解精炼时,粗铜作阳极 | B、生产铝、铜、高纯硅及玻璃过程中都涉及氧化还原反应 | C、黄铜矿冶铜时,副产物SO2可用于生产硫酸,FeO可用作冶炼铁的原料 | D、粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法 |