题目内容
把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,则混合液中微粒浓度关系正确的为( )
| A、c (CH3COO-)<c (Na+) |
| B、c (CH3COOH)+c (CH3COO-)=0.01mol/L |
| C、c (CH3COOH)>c (CH3COO-) |
| D、c (OH-)>c (H+) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:把0.02mol/LCH3COOH和0.01mol/LNaOH以等体积混和,发生反应为CH3COOH+NaOH=CH3COONa+H2O,反应后的溶液中溶质为等浓度的CH3COOH和CH3COONa的混合溶液,依据所学可知醋酸电离程度大于醋酸根离子水解,等浓度的混合溶液显酸性,
A.溶液中一定满足电荷守恒,根据电荷守恒进行判断;
B.溶液中遵循物料守恒,根据物料守恒判断;
C.醋酸的电离程度大于醋酸根离子的水解程度,据此判断醋酸与醋酸根离子的浓度大小;
D.醋酸的电离程度大于醋酸根离子的水解程度,溶液显示酸性,则c(H+)>c(OH-).
A.溶液中一定满足电荷守恒,根据电荷守恒进行判断;
B.溶液中遵循物料守恒,根据物料守恒判断;
C.醋酸的电离程度大于醋酸根离子的水解程度,据此判断醋酸与醋酸根离子的浓度大小;
D.醋酸的电离程度大于醋酸根离子的水解程度,溶液显示酸性,则c(H+)>c(OH-).
解答:
解:0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,反应后溶质为等浓度的CH3COOH和CH3COONa,
A.由于醋酸电离程度大于醋酸根离子水解,混合溶液显酸性,则c(H+)>c(OH-),根据电荷守恒为c(H+)+c(Na+)=c(OH-)+c(CH3COO-)可知:c(Na+)<c(CH3COO-),故A错误;
B.依据溶液中物料守恒可得:c(Na+)=c(CH3COOH)+c(CH3COO-)=0.01mol/L,故B正确;
C.反应后混合液中溶质为等浓度的CH3COOH和CH3COONa,由于醋酸电离程度大于醋酸根离子水解,则混合液中c(CH3COOH)<c(CH3COO-),故C错误;
D.混合液为等浓度的醋酸和醋酸钠,由于醋酸的电离程度大于醋酸根离子的水解,则溶液呈酸性,则c(H+)>c(OH-),故D错误;
故选B.
A.由于醋酸电离程度大于醋酸根离子水解,混合溶液显酸性,则c(H+)>c(OH-),根据电荷守恒为c(H+)+c(Na+)=c(OH-)+c(CH3COO-)可知:c(Na+)<c(CH3COO-),故A错误;
B.依据溶液中物料守恒可得:c(Na+)=c(CH3COOH)+c(CH3COO-)=0.01mol/L,故B正确;
C.反应后混合液中溶质为等浓度的CH3COOH和CH3COONa,由于醋酸电离程度大于醋酸根离子水解,则混合液中c(CH3COOH)<c(CH3COO-),故C错误;
D.混合液为等浓度的醋酸和醋酸钠,由于醋酸的电离程度大于醋酸根离子的水解,则溶液呈酸性,则c(H+)>c(OH-),故D错误;
故选B.
点评:本题考查了酸碱混合的定性判断、溶液中离子浓度大小比较,题目难度中等,注意掌握酸碱混合的定性判断方法,明确判断溶液中离子浓度大小的常用方法,正确判断反应后的溶质为解答本题的关键,学会电荷守恒、物料守恒、盐的水解原理在比较离子浓度大小中的应用.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
下列说法符合事实的是( )
| A、漂白精的有效成分是NaClO |
| B、碘化钾的水溶液遇淀粉现蓝色 |
| C、硫在空气中燃烧生成SO2,在纯氧中生成SO3 |
| D、漂白精露置空气中变质,既发生氧化反应又发生非氧化还原反应 |
卤代烃RCH2CH2X的化学键如图,则下列说法中正确的是( )
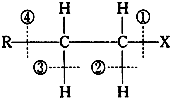

| A、当卤代烃发生水解反应时,被破坏的键是①和④ |
| B、当卤代烃发生水解反应时,被破坏的键是① |
| C、当卤代烃发生消去反应时,被破坏的键是①和③ |
| D、当卤代烃发生消去反应时,被破坏的键是①和② |
可用Zn+Br2═ZnBr2 设计成蓄电池,其中正极反应是( )
| A、Zn→Zn2++2e- |
| B、Br2+2e-→2Br- |
| C、2Br-→Br2+2e- |
| D、Zn2++2e-→Zn |
下列各组单质中,前者在一定的条件下能将后者从其化合物中置换出来的是( )
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤C、Si ⑥Fe H2.
①Al、Fe ②Cl2、S ③Mg、C ④H2、Cu ⑤C、Si ⑥Fe H2.
| A、只有①③⑥ |
| B、只有②④⑥ |
| C、只有①②③④⑥ |
| D、①②③④⑤⑥ |
 熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池正极电极反应式为:O2+2CO2+4e-═2CO32-.试回答下列问题:
熔融盐燃料电池具有高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池正极电极反应式为:O2+2CO2+4e-═2CO32-.试回答下列问题: