题目内容
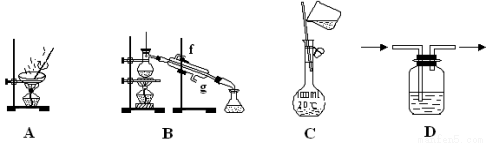
(18分)某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题:

(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)滤液A中若加入过量的铁粉,可能发生的所有离子方程式为 、 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
(1)SiO2 (3分) Fe(OH)3(3分) (2)Fe+2H+= Fe2++H2↑; Fe+2Fe3+=3 Fe2+;(各3分)
(3)过滤(3分) 引流(3分)
【解析】
试题分析:混合物中加入盐酸,SiO2不与盐酸反应,故沉淀是SiO2,滤液中能有FeCl3和AlCl3,加入过量的Na OH,生成沉淀是Fe(OH)3,滤液,中是Na AlO2。(1)沉淀A、B的成分是SiO2 、Fe(OH)3。(2)滤液A中可以和铁粉反应的离子有H+ 和Fe3+,离子方程式为Fe+2H+= Fe2++H2↑; Fe+2Fe3+=3 Fe2+;(3)操作Ⅰ是分离溶液和沉淀的,所以是过滤,过滤中玻璃棒的作用是引流。
考点:物质的基本性质和推断、离子方程式的书写、物质分离的操作。

(15分)某研究小组利用下图装置探究温度对CO还原Fe2O3的影响(固定装置略)
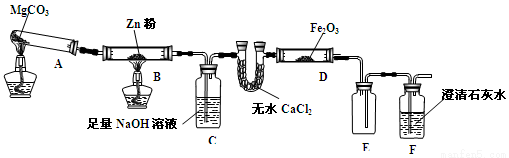
(1)MgCO3的分解产物为 。
(2)装置C的作用是 ,处理尾气的方法为 。
(3)将研究小组分为两组,按题26图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。(Fe2+ 遇K3[Fe(CN)6]溶液会生成蓝色沉淀)
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是 。
②甲组步骤1中反应的离子方程式为 。
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因及其验证方法为 。
④从实验安全考虑,题图装置还可采取的改进措施是 。