题目内容
18.在2L的密闭容器中,充入2molSO2和2molO2,在一定条件下发生反应:2SO2+O2?2SO3,当反应进行了10s时,测得SO3的物质的量为0.8mol,求:(1)10s内SO2、O2的化学反应速率;
(2)SO2的转化率.
分析 2SO2+O2?2SO3
起始浓度(mol/L) 1 1 0
转化浓度(mol/L) 0.4 0.2 0.4
10s时浓度(mol/L) 0.6 0.8 0.4
以此解答该题
解答 解:2SO2+O2?2SO3
起始浓度(mol/L) 1 1 0
转化浓度(mol/L) 0.4 0.2 0.4
10s时浓度(mol/L) 0.6 0.8 0.4
(1)用SO2表示该化学反应速率为$\frac{0.4mol/L}{10s}$=0.04mol/(L•s),
用O2表示该化学反应速率为$\frac{0.2mol/L}{10s}$=0.02mol/(L•s),
答:10s内SO2、O2的化学反应速率分别为0.04mol/(L•s)、0.02mol/(L•s);
(2)SO2的转化率为$\frac{0.4}{1}×100%$=40%,
故答案为:SO2的转化率为40%.
点评 本题考查化学平衡的计算,为高频考点,题目难度中等,注意三段式计算方法的运用,明确转化率、物质的量浓度等物理量的概念及表达式,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
10.碱式碳酸铜是一种用途广泛的化工原料.工业上可用酸性刻蚀废液(主要成分有Cu2+、Fe2+、Fe3+、H +、Cl-)制备,其制备过程如下:
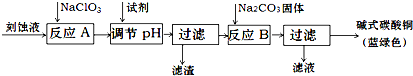
Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
(1)氯酸钠的作用是将Fe2+氧化成Fe3+并最终除去;滤渣的主要成分是Fe(OH)3(写化学式).
(2)调节反应A后溶液的pH范围应为3.2-4.2.可以选择的试剂是d(填序号).
a.氨水 b.稀硫酸 c.氢氧化钠 d.碳酸铜
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的杂质是CuO .(写化学式)
(4)过滤得到的产品洗涤时,如何判断产品已经洗净?取最后一次洗涤液,加入硝酸银和稀硝酸,无沉淀生成则表明已洗涤干净,其它合理答案也给分.
(5)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀.
①若沉淀只有CuCO3,则相应的离子方程式为Cu2++CO32-=CuCO3↓
②若沉淀只有Cu(OH)2,用相应的离子方程式表示其过程Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
③若生成Cu(OH)2和CuCO3的混合物(即碱式盐).则说明碳酸铜于氢氧化铜的溶解度相近
(6)碱式碳酸铜组成可表示为:aCuCO3•bCu(OH)2•cH2O,现通过下列方案测定其组成.步骤如下:
①称量样品;②高温分解;③测出CO2的质量;④测出水蒸汽的质量;⑤称量CuO.
请对上述测定方案作出评价.①称量样品的质量必须知道,③测出CO2的质量④测出水蒸汽的质量⑤称量CuO的质量三个数据知道其中的任意两个即可,另一部分的数据可由样品的质量和已知两部分的质量求得..

Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
(2)调节反应A后溶液的pH范围应为3.2-4.2.可以选择的试剂是d(填序号).
a.氨水 b.稀硫酸 c.氢氧化钠 d.碳酸铜
(3)反应B的温度如过高,则所得蓝绿色产品中可能会出现的杂质是CuO .(写化学式)
(4)过滤得到的产品洗涤时,如何判断产品已经洗净?取最后一次洗涤液,加入硝酸银和稀硝酸,无沉淀生成则表明已洗涤干净,其它合理答案也给分.
(5)将Na2CO3溶液滴入到一定量CuCl2溶液中得到沉淀.
①若沉淀只有CuCO3,则相应的离子方程式为Cu2++CO32-=CuCO3↓
②若沉淀只有Cu(OH)2,用相应的离子方程式表示其过程Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
③若生成Cu(OH)2和CuCO3的混合物(即碱式盐).则说明碳酸铜于氢氧化铜的溶解度相近
(6)碱式碳酸铜组成可表示为:aCuCO3•bCu(OH)2•cH2O,现通过下列方案测定其组成.步骤如下:
①称量样品;②高温分解;③测出CO2的质量;④测出水蒸汽的质量;⑤称量CuO.
请对上述测定方案作出评价.①称量样品的质量必须知道,③测出CO2的质量④测出水蒸汽的质量⑤称量CuO的质量三个数据知道其中的任意两个即可,另一部分的数据可由样品的质量和已知两部分的质量求得..
7.处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S和无毒的气体.已知:
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ•mol-1
②S(g)+O2(g)=SO2(g)△H=-296.0kJ•mol-1
下列说法正确的是( )
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ•mol-1
②S(g)+O2(g)=SO2(g)△H=-296.0kJ•mol-1
下列说法正确的是( )
| A. | CO的燃烧热为566.0 kJ•mol-1 | |
| B. | 反应②△H<0,所以该反应能自发进行 | |
| C. | 使用催化剂能提高其转化率 | |
| D. | 根据①和②推知总反应为2CO(g)+SO2(g)=S(s)+2CO2 (g)△H=-270kJ•mol-1 |
8.下列离子方程式正确的是( )
| A. | 碳酸的电离:H2CO3═2H++HCO3- | |
| B. | 将金属钠加入水中:2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| D. | 向氯化铝溶液中加入过量的烧碱溶液:Al3++3OH-═Al(OH)3↓ |
6.下列说法中正确的是( )


| A. | 酸碱中和反应是放热反应 | |
| B. | 图1所示的反应为吸热反应 | |
| C. | 图2装置中铜片是负极,锌片表面有气泡出现 | |
| D. | 图2装置是将电能转变为化学能的装置 |
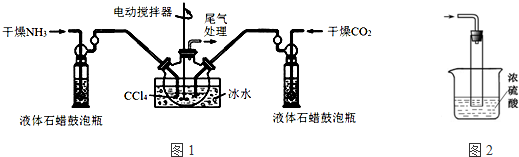
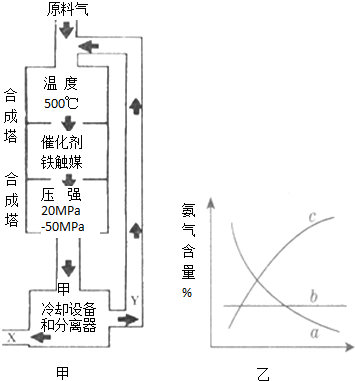 利用所学化学知识解答问题:
利用所学化学知识解答问题: