题目内容
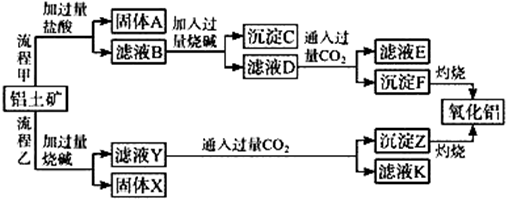
7.用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4•H2O的工艺流程如下:Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度.
(1)步骤Ⅰ中,滤渣的主要成分是二氧化硅.
(2)将MnO2氧化Fe2+的离子方程式补充完整:
□MnO 2+□Fe 2++□═Mn 2++□Fe 3++□□
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、不会引入Cl-,使制得的MnSO4?H2O产品更纯净.
(4)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
步骤Ⅲ中a的取值范围是4.7≤a<7.6.
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度.
已知一定条件下,MnO4-与Mn2+反应生成MnO2.取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为$\frac{1.5y×1{0}^{-4}×55}{x}$.
分析 菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4,生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,过滤除去二氧化硅;向滤液中加入过量MnO2,将亚铁离子氧化为铁离子,本身被还原为二价锰离子,调节滤液pH,使三价铁离子和铝离子沉淀,过滤除去氢氧化铁和氢氧化铝固体,对硫酸锰溶液进行浓缩、冷切结晶、过滤、洗涤干燥得到产品,
(1)二氧化硅不溶于稀硫酸;
(2)根据化合价升降守恒、电荷守恒、原子守恒配平反应;
(3)注意最后不能引入杂质离子,氯气会引入氯离子;
(4)调节滤液pH,使三价铁离子和铝离子沉淀,而锰离子不能沉淀,根据表格回答;
(5)根据方程式3Mn2++2MnO4-+2H2O=5MnO2+4H+进行计算.
解答 解:菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4,生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,;向滤液中加入过量MnO2,将亚铁离子氧化为铁离子,本身被还原为二价锰离子,调节滤液pH,使三价铁离子和铝离子沉淀,过滤除去氢氧化铁和氢氧化铝固体,对硫酸锰溶液进行浓缩、冷切结晶、过滤、洗涤干燥得到产品,
(1)菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2),加入过量稀H2SO4,生成硫酸锰、硫酸亚铁、硫酸铝溶液,二氧化硅不溶解,滤渣的主要成分是二氧化硅,
故答案为:二氧化硅;
(2)锰元素化合价由+4价降低到+2价,铁元素由+2价升高到+3价,根据化合价升降守恒、电荷守恒、原子守恒,配平反应为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O,
故答案为:1、2+4H+、1、2、2H2O;
(3)选用Cl2作为氧化剂会最后的溶液中引入氯离子,使制得的产品不纯,而MnO2不会引入Cl-,使制得的MnSO4?H2O产品更纯净,
故答案为:不会引入Cl-,使制得的MnSO4?H2O产品更纯净;
(4)调节滤液pH,使三价铁离子和铝离子沉淀,根据表格可知二价锰离子开始沉淀的pH=7.6,铝离子开始沉淀的pH=4.7,故4.7≤a<7.6,
故答案为:4.7≤a<7.6;
(5)设含有硫酸锰的物质的量为z,根据方程式
3Mn2++2MnO4-+2H2O=5MnO2+4H+
3mol 2mol
z 0.1y×10-3mol
z=0.15y×10-3mol,
锰元素的质量分数=$\frac{1.5y×1{0}^{-4}×55}{x}$,
故答案为:$\frac{1.5y×1{0}^{-4}×55}{x}$.
点评 本题考查实验制备方案,侧重考查学生对原理及操作的分析评价、对数据的分析运用、物质的分离提纯等,需要学生具备知识的基础,难度中等.

| A. | 发现了元素周期律 | B. | 提出了原子学说 | ||
| C. | 发现了稀有气体 | D. | 提出了分子学说 |
| A. | 石油的分馏是物理变化,得到的各个馏分都是纯净物 | |
| B. | 乙烯、氯乙烯、聚乙烯均可使酸性高锰钾溶液褪色 | |
| C. | CH3CH218OH和CH3COOH反应生成的水的相对分子质量为18 | |
| D. | 石油裂解可以得到乙烯,煤干馏得到的煤焦油中可以提取苯,乙烯和苯使溴水褪色的原理相同 |
| A. | 石油的分馏可得到汽油 | |
| B. | 石油分馏得到的重油经过催化裂化可以得到汽油 | |
| C. | 汽油是烃的混合物,煤油、柴油是由烃构成的纯净物 | |
| D. | 石油裂解是为了获得更多化工原料,如乙烯、丙烯等 |
| A. | 向溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,说明一定含有SO${\;}_{4}^{2-}$ | |
| B. | 向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有气体逸出,说明一定存在CO32-和AlO${\;}_{2}^{-}$ | |
| C. | 用焰色反应检验时,透过蓝色钴玻璃观察火焰呈紫色,则说明含有K+没有Na+ | |
| D. | 取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12,说明不存在NH${\;}_{4}^{+}$、Al3+、Cu2+ |
①将粗氧化铜溶解于稀盐酸中,加热、过滤.调节滤液的pH为3;
②对①所得的滤液按下列步骤进行操作:
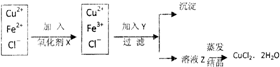
已知:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
(1)加入氧化剂X的目的是:将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离
本实验最合适的氧化剂X是c(填字母)
a.K2Cr2O7 b.NaClO c.H2O2 d.KMnO4
反应的离子方程式是2H++H2O2+2Fe2+=2Fe3++2H2O.
(2)Y可选:CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3,调节pH3.2≤pH<4.7
除去Fe3+的有关离子方程式为CuO+2H+=Cu2++H2O、Fe3++3H2O=Fe(OH)3+3H+
(3)采用低温减压蒸发结晶的方法得到CuCl?2H2O的晶体,还要在过程中不断通入HCl气体,且不能蒸干.
| A. | 氯化氢 | B. | 氢氧化钠 | C. | 酒精 | D. | 氯化钠 |
| A. | MgCl2 | B. | H2O | C. | Ne | D. | NaOH |