��Ŀ����
12���̷���FeSO4•7H2O��������ȱ����ƶѪ����Чҩ������������Ʒ��������м���������������ʣ������̷���һ�ַ�����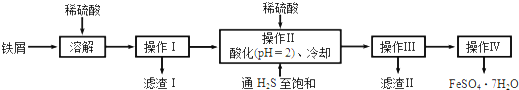
��֪����H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5��
�ش��������⣺
��1�����������������ữ��pH=2��ͨ�����������͵�Ŀ���ǣ�
�ٳ�ȥ����I������Һ�к��е�Sn2+���������ӣ�
��ʹSn2+��ȫ���SnS��������Fe2+��������
�۷�ֹFe2+��������
��2������IV��˳������Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��3������IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ�
�ٳ�ȥ������渽�ŵ���������ʣ�
�ڽ���ϴ�ӹ�����FeSO4•7H2O����ģ�
��4���ⶨ�̷���Ʒ��Fe2+�����ķ����ǣ�a����ȡ8.680g�̷���Ʒ���ܽ⣬��250mL����ƿ�ж��ݣ�b����ȡ25.00mL������Һ����ƿ�У�c���������ữ��0.02000mol/L KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ30.00mL���ζ�ʱ������Ӧ�����ӷ���ʽΪ��5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O����
�ټ���������Ʒ��FeSO4•7H2O����������Ϊ96.08%�����������4λ��Ч���֣���FeSO4•7H2O��Ħ������Ϊ278g/mol��
���������������ⶨ����Ʒ��FeSO4•7H2O����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ��������ԭ���У���Ʒ�д������������ʡ���Ʒ���ֱ�������
���� ��м�������ܽ⣬���������������������������˳�ȥ�������Һ�м���ϡ�����ữ����ͨ�����⣬������SnS��������ֹ�������ӱ����������˷��룬�õ���ҺΪ������������������Ũ������ȴ�ᾧ�����˵Ȳ����ɵõ�FeSO4•7H2O��
��1��ͨ�����������ͣ���ȥ��������Sn2+��������ǿ��ԭ������ԭ�����ӣ���ֹ�������ӱ�������
��2������IV�Ǵ���Һ�������̷����壬��Ҫ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵȣ�
��3������IV�õ����̷�������������ˮϴ�ӣ�ϴȥ�������ʣ��¶Ƚ����̷��ܽ�Ƚ��ͣ������̷��������ʧ��
��4���ٸ��ݷ���ʽ����n��Fe2+������n��FeSO4•7H2O��=n��Fe2+�����ټ���FeSO4•7H2O������������������Ʒ��FeSO4•7H2O������������
����Ʒ�д������������ʣ���H2O��H2SO4�ȣ�����Ʒ���������Ӳ��ֱ������ȣ��ᵼ��FeSO4•7H2O����������ƫ�ͣ�
��� �⣺��м�������ܽ⣬���������������������������˳�ȥ�������Һ�м���ϡ�����ữ����ͨ�����⣬������SnS��������ֹ�������ӱ����������˷��룬�õ���ҺΪ������������������Ũ������ȴ�ᾧ�����˵Ȳ����ɵõ�FeSO4•7H2O��
��1����H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5������������Һ���������ữ��pH=2��Ŀ���ǣ�����ҺPH=2ʱ��Sn2+��ȫ�������������Ӳ�������ͨ�����������͵�Ŀ���ǣ��������ǿ��ԭ�ԣ����Է�ֹ�������ӱ�������
�ʴ�Ϊ��ʹSn2+��ȫ���SnS��������Fe2+����������ֹFe2+��������
��2������IV�Ǵ���Һ�������̷����壬��Ҫ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵȣ�
�ʴ�Ϊ������Ũ�ȡ���ȴ�ᾧ��
��3���̷���������������ʣ���������ˮ����ϴȥ����������������ӣ��¶Ƚ����̷��ܽ�Ƚ��ͣ������̷����ܽ�µ���ʧ��
�ʴ�Ϊ������ϴ�ӹ�����FeSO4•7H2O����ģ�
��4������ 5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O����֪25mL��Һ��n��Fe2+��=5n��MnO4-��=5��0.02000mol/L��0.0300L=0.003mol����250mL��Һ�к�Fe2+=0.003mol��$\frac{250mL}{25mL}$=0.03mol��
n��FeSO4•7H2O��=n��Fe2+��=0.03mol��������=0.03mol��278g/mol=8.34g��
��Ʒ��FeSO4•7H2O������������������=$\frac{8.34g}{8.68g}$��100%=96.08%��
�ʴ�Ϊ��96.08%��
�������������ⶨ����Ʒ��FeSO4•7H2O����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ��������ԭ����ϴ�Ӳ����ף���Ʒ�д������������ʣ���H2O��H2SO4�ȣ������������ӱ������е��������������ȣ�
�ʴ�Ϊ����Ʒ���ֱ�������
���� ���⿼�������Ʊ��������̣��漰���ʵķ����ᴿ����ԭ���ķ������ۡ��������ơ����ʺ����ⶨ�ȣ�ע�����Ŀ��Ϣ���ã���������Ԫ�ػ�����֪ʶ������������ѧ������������ʵ���������Ѷ��еȣ�

| A�� | ���⻯ѧ�������������������ꡱ���γɶ��뵪���������й� | |
| B�� | SiO2������������ά���������ȶ���������ǿ�ᡢǿ�� | |
| C�� | ���ݷ�ɢ����ֱ����С���Խ���ɢϵ��Ϊ��Һ���������Һ | |
| D�� | ��������ͷ���ijЩ����Ԫ�ص����ʵı��� |
| A�� |  ����Cl2 | |
| B�� |  ����100 mL 0.1 mol•L-1 ������Һ | |
| C�� |  ����е����ϴ�Ļ���Һ������ | |
| D�� |  ���뻥�����ܵ�����Һ�� |
| A�� | HO��CH2��2CHO | B�� | HO��CH2��2COOH | C�� | CH3CH2OH | D�� | CH3COOH |
| A�� | ��ϵͳ��������������CH3CH��C2H5��CH��C2H5��CH��CH3��2��������2-��-3��4-���һ����� | |
| B�� | ���ǡ���ά�ص�ˮ����̶��Ǹ߷���ת��ΪС���ӵĹ��� | |
| C�� | ���顢��ȩ�����ᶼ������ͬ���칹�壬����ѣ�CH3OCH3��Ҳ������ͬ���칹�� | |
| D�� | HOCH2COOH�ȿ��Է���ȡ����Ӧ�ֿ��Է������۷�Ӧ |
| A�� | ��Ӧ��Cl2����������KOH�ǻ�ԭ�� | |
| B�� | KCl�ǻ�ԭ���KClO3���������� | |
| C�� | ��Ӧ������3���ȷ��ӹ�ת��6������ | |
| D�� | ����������ԭ���DZ���ԭ����ԭ�ӵ�5�� |
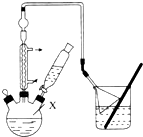 ���嶡������
���嶡������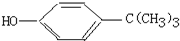 ��ҵ��;�㷺�����������������Է�ȩ��֬���ȶ��������ϵȣ�ʵ�����Ա��ӡ��嶡����[��CH3��3CC1]��Ϊԭ���Ʊ����嶡�����ӣ���֪�嶡�����۵㣨�棩-25.4�е㣨�棩��51
��ҵ��;�㷺�����������������Է�ȩ��֬���ȶ��������ϵȣ�ʵ�����Ա��ӡ��嶡����[��CH3��3CC1]��Ϊԭ���Ʊ����嶡�����ӣ���֪�嶡�����۵㣨�棩-25.4�е㣨�棩��51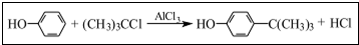 ���÷�Ӧ���ڼ��ң��ų������ȣ���ʹʵ��IJ��ʽ��ͣ����ܵ�ԭ���������嶡���Ȼӷ����²��ʽ��ͣ�
���÷�Ӧ���ڼ��ң��ų������ȣ���ʹʵ��IJ��ʽ��ͣ����ܵ�ԭ���������嶡���Ȼӷ����²��ʽ��ͣ�