题目内容
1.下列各组物质中,按熔点由低到高的顺序排列正确的是( )①Na、K、Rb ②CO、KCl、SiO2 ③O2、I2、Hg ④Na、Mg、Al.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
分析 晶体熔沸点高低顺序是:原子晶体>离子晶体>分子晶体,金属晶体熔沸点差别较大,金属晶体熔沸点与离子半径成反比、与电荷成正比,据此分析解答.
解答 解:①Na、K、Rb原子半径依次增大,则晶体的熔点依次降低,故错误;
②CO为分子晶体,KCl为离子晶体,SiO2为原子晶体,则CO、KCl、SiO2的熔点依次升高,故正确;
③Hg在常温下为液体,I2为固体,则熔点:I2>Hg,故错误;
④为同一周期元素,金属半径逐渐减小,金属键逐渐增强,它们熔点依次升高,故正确.
故选D.
点评 本题考查晶体的熔沸点高低的比较,题目难度不大,注意比较晶体熔沸点高低的角度,侧重于考查学生对基础知识的应用能力

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
12.用等质量铁与稀盐酸反应制备氢气时,欲使生成氢气的化学反应速率增大,下列措施可行的是( )
| A. | 增加铁粒质量 | B. | 换成同浓度的稀硫酸 | ||
| C. | 改成98%的浓硫酸 | D. | 加入纯硝酸 |
6.在正规化学试卷的开始处总有“可能用到的相对原子质量”一项,如H:1 C:12 Cl:35.5 S:32 Cu:64等.请问这些数值准确的说法应该是( )
| A. | 某种核素的相对原子质量 | |
| B. | 某种核素的原子质量 | |
| C. | 某种元素的平均相对原子质量 | |
| D. | 某种元素的平均相对原子质量的近似值 |
13.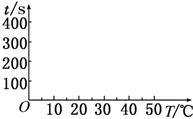 在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
(1)反应的离子方程式是Zn+2H+═Zn2++H2↑,该反应为放热反应(填“放热”或“吸热”).
(2)t1=50s,完成下列时间对温度的曲线图(纵轴表示时间,横轴表示温度).
(3)利用所画的曲线图和相关数据,可得出该反应中温度影响反应速率的规律是温度每升高10℃,反应速率加快到原来的2倍.
(4)t1>(填“>”或“<”)t4,原因是G组中可形成Cu-Zn原电池,发生原电池反应,反应速率加快.
t2>t3(填“>”或“<”),原因是F组中锌为粉末状,表面积较大,反应速率较快.
 在锌与盐酸反应的实验中,某同学得到的结果如下表所示:
在锌与盐酸反应的实验中,某同学得到的结果如下表所示:| 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(2)t1=50s,完成下列时间对温度的曲线图(纵轴表示时间,横轴表示温度).
(3)利用所画的曲线图和相关数据,可得出该反应中温度影响反应速率的规律是温度每升高10℃,反应速率加快到原来的2倍.
(4)t1>(填“>”或“<”)t4,原因是G组中可形成Cu-Zn原电池,发生原电池反应,反应速率加快.
t2>t3(填“>”或“<”),原因是F组中锌为粉末状,表面积较大,反应速率较快.
11.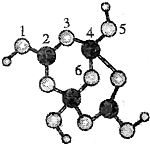 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )
硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )
 硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )
硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:下列叙述正确的是( )| A. | Xm-的化学式为B4O8H42- | |
| B. | 硼原子轨道的杂化类型有sp2、sp3 | |
| C. | 配位键存在于4、6原子之间 | |
| D. | 硼砂晶体中有离子键、配位键两种化学键 |
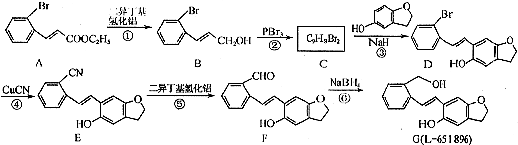
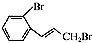 .
.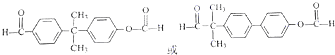 (只写一种).
(只写一种).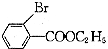 为原料制备二氢异苯并呋喃(结构简式如图
为原料制备二氢异苯并呋喃(结构简式如图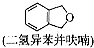 )的合成路线流程图(无机试剂可任选).
)的合成路线流程图(无机试剂可任选).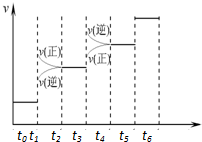 已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.
已知N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ•mol-1.请回答:(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如右图所示.图中tl时引起平衡移动的条件可能是增大压强.其中表示平衡混合物中NH3的含量最高的一段时是t2-t3.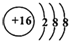 ,该化合物的电子式为
,该化合物的电子式为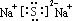 .
.