题目内容
10.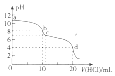 常温下,用0.1mol•L-1的HC1溶液滴定10m L 0.1mol•L-1的Na2CO3溶液,滴定曲线如图所示.下列说法正确的是( )
常温下,用0.1mol•L-1的HC1溶液滴定10m L 0.1mol•L-1的Na2CO3溶液,滴定曲线如图所示.下列说法正确的是( )| A. | 该滴定过程应选择酚酞作指示剂 | |
| B. | a点时,溶液中存在:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| C. | b点时,溶液中存在:c(CO32-)+c(HCO3-)+c( H2CO3)=0.05 mol•L-1 | |
| D. | d点时,溶液中存在电离平衡:H2CO3?2 H++CO32- |
分析 A.滴定终点时溶液的pH=4,应该用甲基橙作指示剂;
B.a点时为碳酸钠溶液,根据碳酸钠溶液中的电荷守恒判断;
C.b点时加入10mL盐酸,反应后溶质为等浓度的碳酸氢钠和NaCl,根据碳酸氢钠溶液中的物料守恒判断;
D.碳酸为二元弱酸,其电离过程分步进行,电离方程式分步书写.
解答 解:A.根据图示曲线可知,达到滴定终点时,溶液的pH=4,呈酸性,应该用甲基橙作指示剂,故A错误;
B.a点时为Na2CO3溶液,根据电荷守恒可知:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B错误;
C.b点时加入10mL 0.1mol•L-1的HC1溶液,反应后生成等浓度的NaHCO3和NaCl,根据NaHCO3溶液中的物料守恒可知:c(CO32-)+c(HCO3-)+c( H2CO3)=0.05 mol•L-1,故C正确;
D.d点加入20mL 0.1mol•L-1的HC1溶液,反应后溶质为碳酸和NaCl,图示为二元弱酸,电离方程式分步书写,正确的电离方程式为:H2CO3?HCO3-+H+、HCO3-?CO32-+H+,故D错误;
故选C.
点评 本题考查了中和滴定、离子浓度大小比较,题目难度中等,明确图象曲线各点对应溶质组成为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20.在生产、保存、运输和使用浓硫酸时,下列说法不正确的是( )
| A. | 工业制取硫酸过程中生成的SO2可循环使用 | |
| B. | 常温下可选用铁制或铝制容器盛装 | |
| C. | 盛装容器的标签上应标注氧化剂和腐蚀品 | |
| D. | 使用时向其中直接加水可制得稀硫酸 |
18.下列关于有机化合物的说法正确的是( )
| A. | 以淀粉为原料可制取乙酸乙酯 | B. | 聚氯乙烯分子中含碳碳双键 | ||
| C. | 丁烷有3种同分异构体 | D. | 油脂的皂化反应属于加成反应 |
15.用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 9.2g甲苯和丙三醇的混合物中,含氢原子数目为0.8NA | |
| C. | 用惰性电极电解1L浓度均为0.2mol/L的Cu(NO3)2和AgNO3的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 | |
| D. | 电解精炼铜(粗铜含铁、锌、银、金杂质)时,每转移2NA个电子,阴极析出1 mol Cu |
2.使溶液中Al3+完全转化成Al(OH)3,应该选择的最好试剂是( )
| A. | HCl | B. | H2SO4 | C. | 氨水 | D. | NaOH |
19.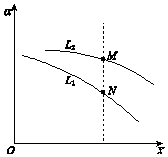 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )| A. | X表示温度 | B. | L2>L1 | C. | 反应速率 υ(M)>υ(N) | D. | 平衡常数 K(M)>K(N) |
20.在多电子原子中,决定轨道能量的是( )
| A. | 电子层 | B. | 电子层和能级 | ||
| C. | 电子层、能级和原子轨道空间分布 | D. | 原子轨道空间分布和电子自旋方向 |