题目内容
硫酸亚铁(FeSO4?7H2O)是一种重要的食品和饲料添加剂.实验室通过如下实验由废铁屑制备FeSO4?7H2O晶体:①将5% Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;⑤将制得的FeSO4?7H2O晶体放在一个小广口瓶中,密闭保存.
请回答下列问题:
(1)写出Fe2+的核外电子排布式 ;
(2)用轨道表示式表示Fe3+的3d电子的排布情况 ;
(3)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,其化学方程式为 ;
(4)硫酸亚铁制备中实验步骤①的目的是 .
请回答下列问题:
(1)写出Fe2+的核外电子排布式
(2)用轨道表示式表示Fe3+的3d电子的排布情况
(3)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,其化学方程式为
(4)硫酸亚铁制备中实验步骤①的目的是
考点:铁的氧化物和氢氧化物,原子核外电子排布,物质分离、提纯的实验方案设计
专题:元素及其化合物
分析:(1)铁是26号元素,铁原子核外有26个电子,铁原子失去2个电子变成亚铁离子,根据构造原理写出亚铁离子核外电子排布式;
(2)根据铁离子的核外电子数,结合能量最低原则、泡利不相容原理和洪特规则,写出核外电子排布式,然后根据3d轨道含有的电子数写出其3d电子的排布情况;
(3)根据“Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl”写出该反应的化学方程式;
(4)根据碳酸钠溶液为碱性溶液,能够除去油污进行分析.
(2)根据铁离子的核外电子数,结合能量最低原则、泡利不相容原理和洪特规则,写出核外电子排布式,然后根据3d轨道含有的电子数写出其3d电子的排布情况;
(3)根据“Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl”写出该反应的化学方程式;
(4)根据碳酸钠溶液为碱性溶液,能够除去油污进行分析.
解答:
解:(1)铁是26号元素,铁原子核外有26个电子,铁原子失去2个电子变成亚铁离子,Fe2+在基态时,核外电子排布式为:[Ar]3d6,
故答案为:[Ar]3d6;
(2)Fe最外层电子数为26,失去3个电子后,核外电子数变为23,由于先失去最外层电子,可写出铁离子最外层电子排布式为:1s22s22p63s23p63d5,所以3d轨道含有5个电子,根据洪特规则,电子总是优先占据1个轨道,并且自旋方向相同,所以Fe3+的3d电子的排布情况是: ,
,
故答案为: ;
;
(3)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,反应的化学方程式为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O,
故答案为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;
(4)Na2CO3溶液显碱性,可以除去铁屑上的油污,升高温度,促进了Na2CO3的水解,溶液碱性增强,去油污能力增强,
故答案为:除去铁屑上的油污.
故答案为:[Ar]3d6;
(2)Fe最外层电子数为26,失去3个电子后,核外电子数变为23,由于先失去最外层电子,可写出铁离子最外层电子排布式为:1s22s22p63s23p63d5,所以3d轨道含有5个电子,根据洪特规则,电子总是优先占据1个轨道,并且自旋方向相同,所以Fe3+的3d电子的排布情况是:
 ,
,故答案为:
 ;
;(3)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,反应的化学方程式为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O,
故答案为:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O;
(4)Na2CO3溶液显碱性,可以除去铁屑上的油污,升高温度,促进了Na2CO3的水解,溶液碱性增强,去油污能力增强,
故答案为:除去铁屑上的油污.
点评:本题考查了核外电子排布式、化学方程式的书写、物质的分离与提纯实验方案设计的评价,题目难度不大,注意掌握化学方程式、核外电子排布式的书写原则,试题有利于提高学生的分析、理解能力.

练习册系列答案
相关题目
下列化合物中,不属于酯类的是( )
A、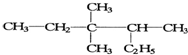 |
| B、CH3CH2NO2 |
C、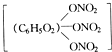 |
D、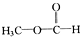 |
下表为部分短周期元素化合价及其相应原子半径的数据.下列说法正确的是( )
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合价 | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合价 | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
| A、C为硫元素 |
| B、A、B是同周期元素 |
| C、F、H的简单离子的电子层结构相同 |
| D、元素G在周期中的位置是第二周期第Ⅳ族 |
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满.若发现92号元素,请在“元素大厦”中安排好它的“房间”( )
| A、第七周期第ⅢB族 |
| B、第六周期第ⅡA族 |
| C、第八周期第ⅠA族 |
| D、第七周期第ⅥB族 |
 如图有机物A的分子,所含有的官能团的名称是
如图有机物A的分子,所含有的官能团的名称是
 ,请按要求回答下列问题:
,请按要求回答下列问题: