题目内容
8.设阿伏加德罗常数为NA,下列说法中正确的是(Mg-24 H-1 O-16)( )| A. | 18g H2O含有的电子数8NA | |
| B. | 常温常压下,1L0.2mol/L MgCl2溶液中含Cl-数为0.2NA | |
| C. | 常温常压下,22.4L的氧气中含氧原子数为2NA | |
| D. | 2.4g的Mg粉与足量的盐酸反应失去电子数为0.2NA |
分析 A、求出水的物质的量,然后根据水中含10个电子来计算;
B、求出氯化镁的物质的量,然后根据氯化镁中含2个氯离子来分析;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、求出镁的物质的量,然后根据镁反应后变为+2价来分析.
解答 解:A.18g水的物质的量为1mol,1mol水中含有10mol电子,含有的电子数10NA,故A错误;
B.1L 0.2mol/L MgCl2溶液中含有0.2mol氯化镁,0.2mol氯化镁中含有0.4mol氯离子,含Cl-数为0.4NA,故B错误;
C.常温常压下,Vm≠22.4L/mol,无法计算氧气的物质的量,故C错误;
D.2.4g镁的物质的量为0.1mol,0.1mol镁与足量盐酸反应生成0.1mol氢气,失去0.2mol电子,反应失去电子数为0.2NA,故D正确;
故选D
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
17.工业上冶炼下列金属,必须另加还原剂的是( )
| A. | Al | B. | Fe | C. | Cu | D. | Ag |
16.下列化合物既能与稀盐酸反应又能与NaOH溶液反应的是( )
①Al
②(NH4)2CO3
③Al2O3
④Ca(HCO3)2
⑤AgNO3
⑥Al(OH)3.
①Al
②(NH4)2CO3
③Al2O3
④Ca(HCO3)2
⑤AgNO3
⑥Al(OH)3.
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③④⑤⑥ | D. | ①②③⑥ |
3.2017年5月18日上午中国国土资源部地质调查局宣布,我国正在南海进行的可燃冰(CH4•nH2O)试采获得成功,这也标志着我国成为全球第一个实现了在海域可燃冰试开采中获得连续稳定产气的国家.则下列有关可燃冰的说法中不正确的是( )
| A. | 可燃冰释放的甲烷属于烃 | |
| B. | 可燃冰是一种洁净的新能源 | |
| C. | 可燃冰实质是水变成的固态油 | |
| D. | 可燃冰燃烧实现了化学能转化为热能 |
13.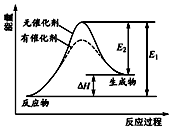 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A. | 加入催化剂,减小了反应的热效应 | |
| B. | 催化剂能降低反应的活化能 | |
| C. | 该反应的△H=E2-E1 | |
| D. | 该图可以表示燃料燃烧反应的能量变化 |
20.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示,若Y原子的最外层电子数是次外层电子数的3倍.下列说法错误的是( )
| X | Y | ||
| Z | W |
| A. | 气态氢化物的热稳定性:X<Y | |
| B. | 最高价氧化物对应水化物的酸性:W>Z>X | |
| C. | X、Y元素均存在同素异形体 | |
| D. | W的单质具有漂白性,能使干燥的有色布条褪色 |
1.下列措施或事实不能用勒沙特列原理解释的是( )
| A. | H2、I2(g)、HI平衡混合气体加压后颜色变深(已知:H2+I2?2HI) | |
| B. | 棕红色的NO2加压后颜色先变深后变浅(已知:2NO2 (g)?N2O4 (g)) | |
| C. | 工业上生产硫酸的过程中,使用过量的空气以提高SO2的利用率 | |
| D. | 滴加酚酞的氨水中加入氯化铵固体后红色变浅 |
2.正确掌握化学用语是学好化学的基础,下列有关化学用语表示正确的是( )
| A. | 中子数为10的氧原子:${\;}_{18}^{10}$O | B. | Na2S的电子式: | ||
| C. | 乙酸的球棍模型: | D. | 葡萄糖的结构简式:C6H12O6 |
