题目内容
配平化学方程式
![]() KMnO4+FeS+H2SO4――MnSO4+Fe2(SO4)3+S↓+K2SO4+H2O
KMnO4+FeS+H2SO4――MnSO4+Fe2(SO4)3+S↓+K2SO4+H2O
答案:6 10 24――6 5 10 3 24
![]() 解析:① 标价态。
解析:① 标价态。
![]() K
K![]() O4+
O4+![]() +H2SO4――
+H2SO4――![]() SO4+
SO4+![]() (SO4)3+
(SO4)3+![]() ↓+K2SO4+H2O
↓+K2SO4+H2O
![]() ② 列变化,算出一个氧化剂(或还原剂)“分子”的化合价总共降低(或升高)多少.
② 列变化,算出一个氧化剂(或还原剂)“分子”的化合价总共降低(或升高)多少.
![]()
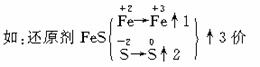
![]() 氧化剂KMnO4,
氧化剂KMnO4,![]() →
→![]() ↓5价
↓5价
![]() ③ 等升降。↑3×5(系数)5FeS;↓5×3(系数)3KMnO4并确定相应的其他元素的系数:
③ 等升降。↑3×5(系数)5FeS;↓5×3(系数)3KMnO4并确定相应的其他元素的系数:
![]() 3KMnO4+5FeS+H2SO4――3MnSO4+Fe2(SO4)3+5S↓+K2SO4+H2O
3KMnO4+5FeS+H2SO4――3MnSO4+Fe2(SO4)3+5S↓+K2SO4+H2O
![]() ④ 平系数。
④ 平系数。
![]() 用观察法配平其他物质的系数,一般先配盐,再配酸,最后配水,并核对氧原子数。
用观察法配平其他物质的系数,一般先配盐,再配酸,最后配水,并核对氧原子数。
![]() ⑤ 验结果。
⑤ 验结果。

练习册系列答案
相关题目