题目内容
20.含某元素的物质间能实现如图直接转化,该元素是( )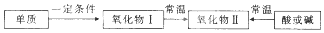
| A. | 钠 | B. | 碳 | C. | 氮 | D. | 硫 |
分析 根据转化图氧化物在常温下能转化为另一种氧化物的是一氧化氮到二氧化氮的转化,其他氧化物如一氧化碳、二氧化硫转化为二氧化碳、三氧化硫都需要条件,据此来回答.
解答 解:A、金属钠对应的碱即为氢氧化钠,在常温下不会转化为过氧化钠,故A错误;
B、碳单质的氧化物一氧化碳转化为二氧化碳需要点燃,常温下不能进行,故B错误;
C、氮气和氧气在闪电条件下转化为一氧化氮,一氧化氮常温下迅速变为二氧化氮,二氧化氮可以用浓硝酸来制取,故C正确;
D、硫单质燃烧生成的二氧化硫在高温高压催化剂作用下才转化为三氧化硫,常温下不能进行,故D错误.
故选C.
点评 本题考查学生元素以及化合物性质知识,注意变价元素所在的物质的性质是解题关键,难度不大.

练习册系列答案
相关题目
8.下列电子式书写不正确的是( )
| A. | 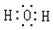 | B. | 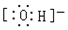 | C. | 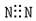 | D. | 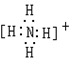 |
15.分子式为C5H10O2,且可以发生水解反应的同分异构体有( )种.
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
5.下列不属于混合物的是( )
| A. | 液氯 | B. | 漂白粉 | C. | 盐酸 | D. | 碘酒 |
9.由一种阳离子和两种酸根离子组成的盐称为混盐.下列关于混盐Na4S2O3的有关判断,不正确的是( )
| A. | 该混盐能使高锰酸钾酸性溶液褪色 | |
| B. | 该混盐溶液加入BaCl2可以生成沉淀 | |
| C. | 该混盐与H2SO4反应有气体生成 | |
| D. | 该混盐在酸性条件下可生成S,每产生1molS转移1.5NA个电子 |
10.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K与温度T的关系如表:
请回答下列问题:
(1)该反应为吸热反应.(填“吸热”或“放热”)
(2)830℃,c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L,c(H2)=0.05mol/L,该反应否(填“是”或“否”)达到的化学平衡状态.
(3)800℃时,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L,c(H2)=0.05mol/L,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为$\frac{1}{3}$,H2的转化率为$\frac{2}{3}$(用分数表示).若再充入1mol H2则H2的转化率为减小(增大,减少,不变)
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应.(填“吸热”或“放热”)
(2)830℃,c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L,c(H2)=0.05mol/L,该反应否(填“是”或“否”)达到的化学平衡状态.
(3)800℃时,固定容积的密闭容器中,放入混合物,起始浓度为c(CO)=0.01mol/L,c(H2O)=0.03mol/L,c(CO2)=0.01mol/L,c(H2)=0.05mol/L,则反应开始时,H2O的消耗速率比生成速率小(填“大”、“小”或“不能确定”)
(4)830℃时,在1L的固定容积的密闭容器中放入2mol CO2和1mol H2,平衡后CO2的转化率为$\frac{1}{3}$,H2的转化率为$\frac{2}{3}$(用分数表示).若再充入1mol H2则H2的转化率为减小(增大,减少,不变)