题目内容
agH2O中质子数为n个,则阿伏伽德罗常数的值可表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量的相关计算
专题:
分析:根据n=
计算出水的物质的量,每个水分子含有10个质子,质子物质的量为水的10倍,再根据N=n?NA计算阿伏伽德罗常数.
| m |
| M |
解答:
解:ag水的物质的量=
=
mol,每个水分子含有10个质子,质子物质的量为水的10倍,则:
mol×10×NAmol-1=n,则NA=
,故选D.
| ag |
| 18g/mol |
| a |
| 18 |
| a |
| 18 |
| 9n |
| 5a |
点评:本题考查阿伏伽德罗常数有关计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
根据热化学方程式S(g)+O2═SO2(g);△H=-297.23kJ/mol下列说法中正确的是( )
| A、S(g)+O2═SO2(1);|△H|>297.3kJ/mol |
| B、S(g)+O2═SO2(1);|△H|<297.3kJ/mol |
| C、1molSO2的键能总和小于1molS和1molO2键能之和 |
| D、1molSO2的键能总和等于1molS和1molO2键能之和 |
下列物质中,不属于“城市空气质量日报”报道内容的是( )
| A、悬浮颗粒 |
| B、氮氧化物 |
| C、CO2 |
| D、SO2 |
常温下,某无色透明的溶液中,下列各组离子能够大量共存的是( )
| A、H+、Na+、Cl-、CO32- |
| B、Ba2+、Na+、SO42-、Cl- |
| C、MnO4-、K+、I-、H+ |
| D、Mg2+、Cl-、NO3-、H+ |
已知VmLAl2(SO4)3溶液中含有Al3+ag取出
mL溶液稀释到4VmL,则稀释后溶液中SO42-的物质的量浓度为( )
| V |
| 2 |
A、
| ||
B、
| ||
C、
| ||
| D、125a/54Vmol/L |
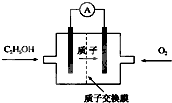 目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A、通入乙醇的电极为该电池的正极 |
| B、放电过程中,电源内部的H+从正极区向负极区迁移 |
| C、该电池的正极反应为:4H++O2+4e-=2H2O |
| D、用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A、同压强、同温度的O2和O3 |
| B、同温度、同体积的NH3和N2 |
| C、同体积、同密度的C2H4和C3H6 |
| D、同压强、同体积的N2O和CO2 |
需加入氧化剂才能实现的是( )
| A、Fe3+→Fe2+ |
| B、Cl-→Cl2 |
| C、CuO→Cu |
| D、H2SO4→BaSO4 |
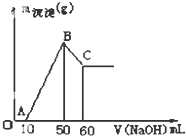 把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.
把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.