题目内容
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、2.4 g 金属镁变成镁离子时失去的电子数为0.1NA |
| B、2 g 氢气中含有的分子数为NA |
| C、3.01×1023 个氮分子中含有的原子数为2NA |
| D、22.4L氨气中含有的原子数为3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.镁为2价金属,2.4g镁的物质的量为0.1mol,完全反应失去0.2mol电子;
B.氢气的摩尔质量为2g/mol,2g氢气的物质的量为1mol;
C.氮气为双原子分子,3.01×1023 个氮分子的物质的量为0.5mol,含有1mol氮原子;
D.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氨气的物质的量.
B.氢气的摩尔质量为2g/mol,2g氢气的物质的量为1mol;
C.氮气为双原子分子,3.01×1023 个氮分子的物质的量为0.5mol,含有1mol氮原子;
D.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氨气的物质的量.
解答:
解:A.2.4g镁的物质的量为0.1mol,0.1molMg完全反应失去0.2mol电子,失去的电子数为0.2NA,故A错误;
B.2g氢气的物质的量为1mol,含有的分子数为NA,故B正确;
C.3.01×1023 个氮分子的物质的量是0.5mol,0.5mol氮气中含有1mol氮原子,含有的原子数为NA,故C错误;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氨气的物质的量,故D错误;
故选B.
B.2g氢气的物质的量为1mol,含有的分子数为NA,故B正确;
C.3.01×1023 个氮分子的物质的量是0.5mol,0.5mol氮气中含有1mol氮原子,含有的原子数为NA,故C错误;
D.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氨气的物质的量,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
下列分散系中,能出现丁达尔现象的是( )
| A、蔗糖溶液 | B、碘化银沉淀 |
| C、浓盐酸 | D、豆浆 |
如图所示的实验方法、装置或操作完全正确的是( )
A、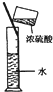 稀释浓H2SO4 |
B、 萃取时振荡 |
C、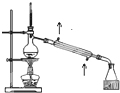 石油的蒸馏 |
D、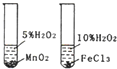 研究不同催化剂对反应速率的影响 |
a克铁粉与含有硫酸的硫酸铜溶液完全反应后,得到a克铜,则参加反应的硫酸铜与硫酸的物质的量之比是( )
| A、1:7 | B、7:1 |
| C、7:8 | D、8:7 |
下列有关反应热的叙述正确的是( )
| A、已知2H2(g)+O2(g)2H2O(g);△H=483.6kJ/mol,则氢气的燃烧热为241.8kJ |
| B、在测定中和热的实验中,盐酸物质的量一般要大于氢氧化钠物质的量,这样才能保证氢氧化钠中和完全 |
| C、已知碳的燃烧热为 y KJ/mol,当7.2 g 的碳在12.8 g 的氧气中燃烧,至反应物耗尽并放出x KJ 的热量,则可求出 1 mol 碳与氧气反应生成一氧化碳时△H=(0.5 y-2.5x)KJ/mol |
| D、己知2C(s)+2O2(g)=CO2(g);△H1 2C(s)+O2(g)=CO(g);△H2 则△H1>△H2 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时不应将溶液直接蒸干 |
| D、食盐应放在滤纸上称量 |
下列各组有机物,一定属于同系物的是( )
A、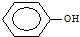 和 和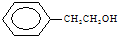 |
| B、最简式相同的有机物 |
| C、丙酸丙酯和高级脂肪甘油脂 |
| D、分子组成为CnH2n+2和CmH2m+2(m≠n)的两种烃 |
下列电离方程式错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na++H++SO42- |
| C、H2CO3=2H++CO32- |
| D、HNO3=H++NO3- |
