题目内容
11.有由MgO、Al2O3、SiO2、Fe2O3组成的混合粉末.现取两份该混合粉末试样进行试验.(1)将一份混合粉末溶于过量的盐酸,得到沉淀X和滤液Y,沉淀X为SiO2,滤液Y中含有的阳离子主要是Mg2+、Al3+、Fe3+、H+,向滤液Y中加入过量NaOH溶液,得到的沉淀是Fe(OH)3、Mg(OH)2.
(2)将另一份混合粉末溶液过量NaOH溶液,发生反应的离子方程式为Al2O3+2OH-═2AlO2-+H2O、SiO2+2OH-═SiO32-+H2O.
分析 (1)由MgO、Al2O3、SiO2、Fe2O3组成的混合粉末,加盐酸只有SiO2不反应,过滤后滤液含Mg2+、Al3+、Fe3+、H+,加过量NaOH生成的沉淀为氢氧化镁、氢氧化铁;
(2)另一份混合粉末溶液过量NaOH溶液,只有Al2O3、SiO2发生反应,以此来解答.
解答 解:(1)由MgO、Al2O3、SiO2、Fe2O3组成的混合粉末,加盐酸只有SiO2不反应,则沉淀X为SiO2,MgO、Al2O3、Fe2O3均与盐酸反应,过滤后滤液含Mg2+、Al3+、Fe3+、H+,因氢氧化铝能溶于强碱,则加过量NaOH生成的沉淀为Fe(OH)3、Mg(OH)2,
故答案为:SiO2;Mg2+、Al3+、Fe3+、H+;Fe(OH)3、Mg(OH)2;
(2)另一份混合粉末溶液过量NaOH溶液,只有Al2O3、SiO2发生反应,发生的离子反应为Al2O3+2OH-═2AlO2-+H2O、SiO2+2OH-═SiO32-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O、SiO2+2OH-═SiO32-+H2O.
点评 本题考查常见金属氧化物的性质,为高考常见题型,侧重于元素化合物知识的综合应用,题中注意氧化铝和二氧化硅的性质,题目难度不大.

练习册系列答案
相关题目
2.下列各组名词或现象中,三者间没有逐级因果关系的是( )
| A. | 氟氯代烷--臭氧空洞--皮肤癌患者增多 | |
| B. | 汽车尾气--光化学污染--咳嗽和气喘患者增多 | |
| C. | 人口增多--空气中CH4的浓度增大--温室效应 | |
| D. | 含磷洗衣粉--水体富营养化--水栖生物大量死亡 |
20.关天单键、双键、叁键的说法正确的是( )
| A. | 单键的键长最短,键能最大 | |
| B. | 叁键的键长最短,键能最大 | |
| C. | 双键中两个键都活泼,加成时都断裂 | |
| D. | 只有碳原子间才能形成双键和叁键 |
6.下列有机化合物中,可以看作醇类的是( )
| A. | 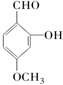 | B. |  | ||
| C. | 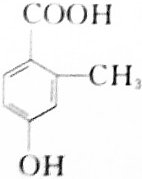 | D. | 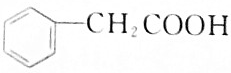 |
6.在一密闭容器中,反应aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则( )
| A. | 平衡逆向移动了 | B. | 物质A的转化率减小了 | ||
| C. | 物质B的质量分数增大了 | D. | 反应速率增大,且v正>v逆 |
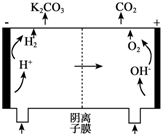 为实现CO2减排,热钾碱法化学吸收CO2在合成氨、制氢、天然气等石油化工行业中应用广泛.该方法的原理是用碳酸钾溶液吸收CO2生成碳酸氢钾(称富液)来脱除CO2.之后高温加热富液,使碳酸氢钾分解释放CO2生成碳酸钾,溶液循环使用.某研究小组用500mL 1mol/L K2CO3溶液吸收5.6L 的CO2(标准状况)形成富液(忽略溶液体积变化).
为实现CO2减排,热钾碱法化学吸收CO2在合成氨、制氢、天然气等石油化工行业中应用广泛.该方法的原理是用碳酸钾溶液吸收CO2生成碳酸氢钾(称富液)来脱除CO2.之后高温加热富液,使碳酸氢钾分解释放CO2生成碳酸钾,溶液循环使用.某研究小组用500mL 1mol/L K2CO3溶液吸收5.6L 的CO2(标准状况)形成富液(忽略溶液体积变化). bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )
bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )