题目内容
4.NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 11.2 L的戊烷所含的分子数为0.5NA | |
| B. | 28 g乙烯所含共用电子对数目为6NA | |
| C. | 在标准状况,11.2 L三氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、乙炔的混合气体共14 g,其原子数为3NA |
分析 A.标况下,戊烷为液体;
B.求出乙烯的物质的量,然后根据1mol乙烯中含6mol共用电子对来分析;
C.标况下,三氯甲烷为液体;
D.1个乙烯分子含有6个原子,1个乙炔分子含有4个原子;
解答 解:A.标况下,戊烷为液体,不能使用气体摩尔体积,故A错误;
B.乙烯的物质的量n=$\frac{m}{M}$=$\frac{28g}{28g/mol}$=1mol,而1mol乙烯中含6mol共用电子对,故B正确;
C.标况下,三氯甲烷为液体,不能使用气体摩尔体积,故C错误;
D.1个乙烯分子含有6个原子,1个乙炔分子含有4个原子,乙烯与乙炔相对分子质量不同,混合气体共14 g,所含原子个数与乙烯、乙炔所占物质的量之比有关,二者物质的量未知,无法计算所含原子个数,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 碳酸氢钠是焙制糕点的发酵粉的一种成分 | |
| B. | CO、NO、NO2都是大气污染物,在空气中都能稳定存在 | |
| C. | 光导纤维和玻璃都是硅酸盐产品 | |
| D. | 明矾能作净水剂,因为它能与水反应生成强氧化性的氢氧化铝胶体 |
15.下列物质在通常条件下能与氢氧化钠溶液反应的是( )
| A. | 甲烷 | B. | 乙醇 | C. | 苯 | D. | 乙酸 |
12.关于下列物质的用途的说法错误的是( )
| A. | 部分卤代烃可用作灭火剂 | |
| B. | 甲醛的水溶液(福尔马林)可用于防腐 | |
| C. | 酚类化合物有毒,不能用于杀菌消毒 | |
| D. | 乙二醇可用于配制汽车防冻液 |
19.下列表示中不是官能团的是( )
| A. | C=C | B. | C≡C | C. | -CH3 | D. | -X |
20.科学家已经合成了元素周期表上的第113号至第119号元素,${\;}_{114}^{263}$X原子在生成数微秒后会衰变成${\;}_{112}^{258}$Y.下列有关叙述中,正确的是( )
| A. | 114号元素衰变成112号元素是化学变化 | |
| B. | 114号元素位于第12列 | |
| C. | ${\;}_{114}^{263}$X的中子数与质子数之差为149 | |
| D. | 112号元素位于周期表第七周期第ⅡB族 |
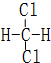 和
和 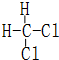 同一种物质.
同一种物质.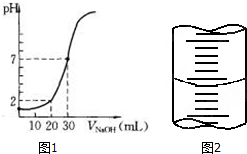 用一定物质的量浓度的NaOH溶液滴定10.00mL已知浓度的盐酸,滴定结果如图1所示.回答下列问题:
用一定物质的量浓度的NaOH溶液滴定10.00mL已知浓度的盐酸,滴定结果如图1所示.回答下列问题: