题目内容
下列物质与HNO3反应时,HNO3既表现强氧化性又表现酸性的是( )
| A、Fe(OH)2 |
| B、CuO |
| C、C |
| D、Cu |
考点:硝酸的化学性质
专题:
分析:硝酸表现氧化性,则反应后N元素的化合价降低;表现出酸性,反应物中有硝酸盐生成.
解答:
解:A.稀硝酸与氢氧化亚铁反应生成硝酸铁、NO和水,N元素化合价降低,硝酸表现出氧化性,生成硝酸铁,硝酸还表现出酸性,故A正确;
B.稀硝酸与氧化铜反应反应生成硝酸铜和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故B错误;
C.浓硝酸与灼热的碳反应生成二氧化碳、二氧化氮和水,硝酸只表现出强氧化性,故C错误;
D.稀硝酸与铜反应生成硝酸铜、NO和水,N元素化合价降低,硝酸表现出氧化性,生成硝酸铜,硝酸还表现出酸性,故D正确;
故选AD.
B.稀硝酸与氧化铜反应反应生成硝酸铜和水,化合价没有变化,不是氧化还原反应,硝酸只表现出酸性,故B错误;
C.浓硝酸与灼热的碳反应生成二氧化碳、二氧化氮和水,硝酸只表现出强氧化性,故C错误;
D.稀硝酸与铜反应生成硝酸铜、NO和水,N元素化合价降低,硝酸表现出氧化性,生成硝酸铜,硝酸还表现出酸性,故D正确;
故选AD.
点评:本题考查硝酸的性质,难度中等.要注意硝酸酸性与氧化性的判断方法.

练习册系列答案
相关题目
清华大学朱令“铊中毒案”一度引发人们对化学药品使用的热议.铊盐与氰化钾被列为A级危险品,铊(Tl)的原子序数为81,ⅢA族元素,则下列推断正确的是( )
| A、Tl+最外层有3个电子 |
| B、氧化性:Tl3+<Al3+ |
| C、Tl(OH)3与Al(OH)3相似,也是两性氢氧化物 |
| D、铊位于第五周期 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2?2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法错误的是( )
| A、使用催化剂是为了加快反应速率,提高生产效率 |
| B、在上述条件下,SO2不可能100%地转化为SO3 |
| C、为了提高SO2的转化率,应适当提高O2的浓度 |
| D、达到平衡时,SO2的浓度与SO3的浓度相等 |
下列关于苯乙烯(结构简式为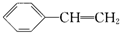 )的叙述,错误的是( )
)的叙述,错误的是( )
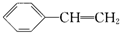 )的叙述,错误的是( )
)的叙述,错误的是( )| A、可以和溴水反应 |
| B、是乙烯的同系物 |
| C、化学式为C8H8 |
| D、1 mol苯乙烯最多可以和4 mol H2发生加成反应 |
下列说法错误的是( )
| A、分子组成为C4H100的醇有4种 |
| B、1 mol二氯乙烷与Cl2发生取代反应,反应完全共需4 mol Cl2 |
| C、(CH3)3CCH2CH3的一氯代物有3种 |
| D、乙烷与Cl2反应与乙烯与C12的反应类型相同 |
下列各组离子在指定的溶液中能大量共存的是( )
| A、在pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B、能溶解Al(OH)3的溶液中:NH4+、SO42-、Cl-、HCO3- |
| C、酚酞呈红色的溶液中:K+、Na+、AlO2-、NO3- |
| D、含有大量Fe2+的溶液中:H+、K+、ClO-、SO42- |
 美国每日科学网站文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分-“表没食子儿茶素没食子酸酯”(EGCG).研究显示,该成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.已知EGCG的结构简式如图,有关EGCG的说法不正确的是( )
美国每日科学网站文章报道:美国梅奥诊所的研究人员发现绿茶含有有助于消灭血癌细胞的成分-“表没食子儿茶素没食子酸酯”(EGCG).研究显示,该成分通过干扰血癌细胞生存所需的信号传递,能使血癌(白血病)中癌细胞自杀性死亡.已知EGCG的结构简式如图,有关EGCG的说法不正确的是( )| A、EGCG分子中含有两个手性碳原子 |
| B、EGCG遇FeCl3溶液能发生显色反应 |
| C、EGCG在空气中不易被氧化 |
| D、EGCG可与氢氧化钠溶液反应 |