题目内容
19.关于下列装置说法正确的是( )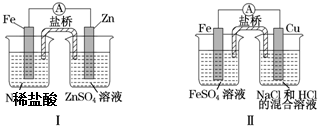
| A. | 装置Ⅰ中铁溶解、锌不溶解,装置Ⅱ中铁溶解、铜不溶解 | |
| B. | 装置Ⅰ中电流表指针不偏转,装置Ⅱ中电流表指针偏转 | |
| C. | 装置Ⅰ和装置Ⅱ中正极反应均是2H++2e-═2H2 | |
| D. | 盐桥中的阳离子均向右侧烧杯移动 |
分析 A、装置Ⅰ中锌与盐酸发生自发的氧化还原反应,所以锌是负极,锌溶解;装置Ⅱ中铁与盐酸发生自发的氧化还原反应;
B、装置Ⅰ和装置Ⅱ都构成原电池,指针都偏转;
C、装置Ⅰ中锌与盐酸发生自发的氧化还原反应,所以锌是负极,锌溶解;装置Ⅱ中铁与盐酸发生自发的氧化还原反应,正极都是氢离子得电子,发生还原反应;
D、装置Ⅰ中正极是右边,装置Ⅱ中右边是正极.
解答 解:A、装置Ⅰ中锌与盐酸发生自发的氧化还原反应,所以锌是负极,锌溶解;装置Ⅱ中铁与盐酸发生自发的氧化还原反应,铁溶解,铜不溶解,故A错误;
B、装置Ⅰ和装置Ⅱ都构成原电池,指针都偏转,故B错误;
C、装置Ⅰ中锌与盐酸发生自发的氧化还原反应,所以锌是负极,锌溶解;装置Ⅱ中铁与盐酸发生自发的氧化还原反应,正极都是氢离子得电子,发生还原反应,电极反应式为:2H++2e-═2H2,故C正确;
D、装置Ⅰ中正极是左边,装置Ⅱ中右边是正极,所以装置Ⅰ盐桥中的阳离子均向左侧烧杯移动,故D错误;
故选:C.
点评 本题考查原电池知识,为高频考点,侧重于学生分析能力和基本理论的理解和运用的考查,注意把握金属的活泼性强弱以及电极方程式的书写,难度不大.

练习册系列答案
相关题目
10.下列说法不正确的是( )
| A. | 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应 | |
| B. | 淀粉、纤维素水解的最终产物均为葡萄糖 | |
| C. | 由甲烷的氯代物有4种,可推知乙烷的氯代物有6种 | |
| D. | 天然油脂没有固定的熔点和沸点,所以天然油脂是混合物 |
7. X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
 X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的气态氢化物的水溶液显酸性 | |
| B. | X的原子半径小于Y | |
| C. | Z的最外层电子数比Y多 | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
14.下列物质中,属于同分异构体的是( )
| A. | C3H8与C4H10 | B. | 正丁烷与异丁烷 | C. | H(氢)与D(重氢) | D. | 金刚石与石墨 |
4.下列有关粒子的表示方法正确的是( )
| A. | 氨气分子的电子式: | B. | 硫原子结构示意图: | ||
| C. | KCl的电子式: | D. | H2O2的电子式: |
11.为了探究外界条件对过氧化氢分解速率的影响.某化学兴趣小组做了以下实验:
回答下列问题:
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;氯化铁\;}}{\;}$2H2O+O2↑.
(2)实验a的目的是探究温度对H2O2分解速率的影响,FeCl3在实验中的作用是催化作用(或催化剂),该实验得出的结论是温度越高,H2O2分解速率越快.
(3)实验b的目的是探究浓度对H2O2分解速率的影响,但未观察到预期的实验现象.为了达到实验目的,请用现有实验中提供的试剂或条件,提出对实验b的改进意见分别在两支试管中加入等量的FeCl3溶液(或将两支试管同时放入盛有相同温度热水的烧杯中).
| 实验编号 | 实验操作 | 实验现象 |
| a | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴1mol•L-1 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡 | 试管A中无明显气泡产生 试管B中出现大量气泡 |
| b | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 两支试管中都未见明显气泡 |
(1)过氧化氢分解的化学方程式为2H2O2$\frac{\underline{\;氯化铁\;}}{\;}$2H2O+O2↑.
(2)实验a的目的是探究温度对H2O2分解速率的影响,FeCl3在实验中的作用是催化作用(或催化剂),该实验得出的结论是温度越高,H2O2分解速率越快.
(3)实验b的目的是探究浓度对H2O2分解速率的影响,但未观察到预期的实验现象.为了达到实验目的,请用现有实验中提供的试剂或条件,提出对实验b的改进意见分别在两支试管中加入等量的FeCl3溶液(或将两支试管同时放入盛有相同温度热水的烧杯中).
8.下列离子方程式书写正确的是( )
| A. | 向NaHSO4溶液中滴Ba(OH)2溶液.恰好使溶液呈中性:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| B. | 镁粉撒入NH4Cl溶液:Mg+2H+═Mg2++H2↑ | |
| C. | 过量SO2通入Ca(ClO)2溶液中:ClO-+SO2+H2O═HSO3-+HClO | |
| D. | 向FeI2溶液中通入等量氯气:2I-+C12═I2+2Cl- |
9.短周期元素A和B可形成AB2型化合物,若B原子序数为m,则A的原子序数为下面算式中的( )
①m+6
②m+8
③m-2
④m-1
⑤m+4
⑥m+14.
①m+6
②m+8
③m-2
④m-1
⑤m+4
⑥m+14.
| A. | ②③⑥ | B. | ①②③④ | C. | ①②⑥ | D. | ①②③④⑤⑥ |