题目内容
2.下列反应的离子方程式书写正确的是( )| A. | 钠与水的反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | 硫酸铝溶液与氨水的反应:Al3++3OH-=Al(OH)3↓ | |
| C. | 氢氧化铜与稀硫酸的反应:OH-+H+=H2O | |
| D. | 铁粉与稀盐酸反应:Fe+2H+=Fe2++H2↑ |
分析 A.电荷不守恒;
B.一水合氨为弱碱应保留化学式;
C.氢氧化铜为沉淀,应保留化学式;
D.二者反应生成氯化亚铁和氢气.
解答 解:A.钠与水的反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.硫酸铝溶液与氨水的反应,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.氢氧化铜与稀硫酸的反应,离子方程式:Cu(OH)2+2H+=2H2O+Cu2+,故C错误;
D.铁粉与稀盐酸反应生成氯化亚铁和氢气,离子方程式:Fe+2H+=Fe2++H2↑,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式的书写方法是解题关键,注意离子反应需遵循客观事实、遵循原子个数、电荷数守恒规律,注意化学式的拆分,题目难度不大.

练习册系列答案
相关题目
13.已知分解1g碳酸镁固体吸收1.366kJ,则它的热化学方程式是( )
| A. | MgCO3(s)═MgO(s)+CO2(g)△H=+1.366 kJ/mol | |
| B. | MgCO3(s)═MgO(s)+CO2(g)△H=-1.366 kJ/mol | |
| C. | MgCO3(s)═MgO(s)+CO2(g)△H=-114.7 kJ/mol | |
| D. | MgCO3(s)═MgO(s)+CO2(g)△H=+114.7 kJ/mol |
10.为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气.下列关于Na2O2的叙述正确的是( )
| A. | Na2O2中阴、阳离子的个数比为1:1 | |
| B. | Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等 | |
| C. | Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的物质的量相等 | |
| D. | Na2O2的漂白原理与活性炭的漂白原理相同 |
17.科学家预言超级原子的发现将会重建周期表,2015年1月美国科学在《Science》是发表论文,宣布发现了A1的超原子结构A113和A114,并在质谱仪检测到稳定的A113I-等,Al13、Al14的性质很像现行周期表中的某主族元素,己知这类超原子当具有40个价电子时最稳定(例Al原子具有3个价电子).下列说法不正确的是( )
| A. | Al14有42个价电子,且与IIA族元素性质相似 | |
| B. | Al13有39个价电子,且与卤素性质类似 | |
| C. | Al13、Al14 互为同素异形体 | |
| D. | Al13原子中存在离子键 |
14.下列物质的稀溶液无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
| A. | Na2CO3和盐酸 | B. | AlCl3和NaOH | C. | NaAlO2和硫酸 | D. | Na2CO3和BaCl2 |
11.下列有关的离子方程式书写正确的是( )
| A. | 氢氧化钡溶液和稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| B. | 碳酸钙和醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4 NH3•H2O═AlO2-+4NH4++2 H2O | |
| D. | 用少量Ca(OH)2与NaHCO3反应:Ca2++2OH-+2HCO3-═CaCO3↓+H2O+CO32- |
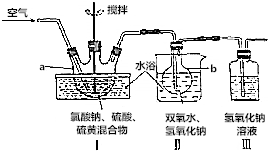
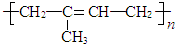 .
.