题目内容
下列表示对应化学反应的离子方程式正确的是( )
| A、金属钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、Cu与浓硝酸反应制NO2:Cu+4HNO3(浓)=Cu2++2NO3-+2NO2↑+2H2O |
| C、向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸2OH-+CO32-+4H+=CO2↑+3H2O |
| D、将NaHSO4与Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷数不守恒;
B.硝酸为强电解质,应拆成离子形式;
C.向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸,反应生成水、氯化钠、二氧化碳;
D.NaHSO4与Ba(OH)2溶液混合至中性反应生成硫酸钠、硫酸钡和水;
B.硝酸为强电解质,应拆成离子形式;
C.向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸,反应生成水、氯化钠、二氧化碳;
D.NaHSO4与Ba(OH)2溶液混合至中性反应生成硫酸钠、硫酸钡和水;
解答:
解:A.金属钠与水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.Cu与浓硝酸反应制NO2,离子方程式:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故B错误;
C.向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸,离子方程式:OH-+CO32-+3H+=CO2↑+2H2O,故C错误;
D.NaHSO4与Ba(OH)2溶液混合至中性反应生成硫酸钠、硫酸钡和水,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确;
故选:D.
B.Cu与浓硝酸反应制NO2,离子方程式:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,故B错误;
C.向等物质的量浓度的NaOH和Na2CO3的混合液中加入稀盐酸,离子方程式:OH-+CO32-+3H+=CO2↑+2H2O,故C错误;
D.NaHSO4与Ba(OH)2溶液混合至中性反应生成硫酸钠、硫酸钡和水,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确;
故选:D.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意离子方程式应遵循原子个数、电荷数守恒、遵循反应的客观事实,注意反应物用量对反应的影响,选项D为易错选项.

练习册系列答案
相关题目
下列有机物的模型中,代表乙烯的是( )
A、 |
B、 |
C、 |
D、 |
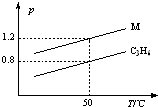 如图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试据图形判断M气体可能是( )
如图中两条曲线分别表示1g C3H6、1g M气体在相同体积的容器中压强和温度的关系,试据图形判断M气体可能是( )| A、SO2 |
| B、CO |
| C、C3H8 |
| D、Cl2 |
下列化合物在水中电离方程式正确的是( )
| A、Ba(OH)2═Ba2++OH2- |
| B、NaHCO3═Na++H++CO32- |
| C、NaHSO4═Na++H++SO42- |
| D、Al2(SO4)3═2Al3++(SO42-)3 |
下列离子方程式书写正确的是( )
| A、碳酸钙与稀盐酸反应:CO32-+2H+=CO2↑+H2O |
| B、氢氧化镁溶于盐酸:Mg(OH)2+2H+=Mg2++2H2O |
| C、铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe3+ |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
下列实验过程中曲线变化正确的是( )


| A、①表示Na2CO3溶液中滴入稀盐酸 |
| B、②表示溴水中滴入Na2SO3溶液 |
| C、③表示AgNO3溶液中滴入氨水 |
| D、④表示一定条件下2SO2+O2?2SO3△H<0达平衡后,升高温度 |
工业上通过2Al2O3+3C+6Cl2═4AlCl3+3CO2制取无水氯化铝,下列说法正确的是( )
| A、AlCl3是氧化产物 |
| B、Cl2是氧化剂 |
| C、每生成1 mol CO2,转移4个电子 |
| D、C发生还原反应 |