题目内容
2. 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液240mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液240mL:(1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为②①③⑧⑤⑥⑦④.本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、还有250mL容量瓶、胶头滴管.
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图. 烧杯的实际质量为27.4g,要完成本实验该同学应称出10.0g NaOH.
(3)使用容量瓶前必须进行的一步操作是检查容量瓶是否漏水.
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是④⑤.
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
分析 (1)依据配制一定物质的量浓度溶液一般步骤排序及选择使用仪器;
(2)依据天平称量固体原理可知:固体质量=砝码的质量+游码的质量,右盘中砝码为20g,5g,游码质量2.4g;依据m=CVM计算需要溶质的质量;
(3)容量瓶带有活塞,使用过程中需要上下颠倒,所以使用前应检查是否漏水;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶、贴标签,所以正确的顺序为:②①③⑧⑤⑥⑦④;用到的仪器依次为:托盘天平、药匙、玻璃棒、烧杯、容量瓶和胶头滴管,要配制1.0mol•L-1的NaOH溶液240mL,应选择250mL容量瓶,所以还缺少的仪器:250mL容量瓶、胶头滴管;
故答案为:②①③⑧⑤⑥⑦④;250mL容量瓶、胶头滴管;
(2)依据天平称量固体原理可知:固体质量=砝码的质量+游码的质量,右盘中砝码为20g,5g,游码质量2.4g,所以烧杯的实际质量为27.4g;配制1.0mol•L-1的NaOH溶液240mL,应选择250mL容量瓶,配制250mL溶液,需要氢氧化钠质量m=1.0mol/L×40g/mol×0.25L=10.0g;
故答案为:27.4;10.0;
(3)容量瓶带有活塞,使用过程中需要上下颠倒,所以使用前应检查是否漏水;
故答案为:检查容量瓶是否漏水;
(4)①没有洗涤烧杯和玻璃棒,导致溶质部分损耗,溶质的物质的量偏小,溶液浓度偏低,故不选;
②转移溶液时不慎有少量洒到容量瓶外面,导致溶质部分损耗,溶质的物质的量偏小,溶液浓度偏低,故不选;
③容量瓶不干燥,含有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故不选;
④定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故选;
⑤未冷却到室温就将溶液转移到容量瓶并定容,冷却后,液面下降,溶液体积偏小,溶液浓度偏高,故选;
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故不选;
故选:④⑤;
故答案为:④⑤.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意容量瓶规格选择及使用方法,题目难度不大.

 名校课堂系列答案
名校课堂系列答案| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | A | B | ||||||
| 3 | C | D | E | F | H | |||
| 4 | G | R |
(2)E元素的最高价氧化物对应的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(3)D、E、A三种元素按原子半径由大到小的顺序排列的是Mg>Al>C(用元素符号表示);
(4)B元素最常见的氢化物的化学式是H2O,该氢化物在常温下跟G发生反应的化学方程式是2K+2H2O=2KOH+H2↑,所得溶液的pH>7(填“>”、“<”或“=”);
(5)R元素跟C元素形成的化合物的化学式是NaBr,高温灼烧该化合物时,火焰呈黄色;
(6)F和R元素两者核电荷数之差是18.
| A. | A、B可能属同一周期 | |
| B. | A位于B的前一周期 | |
| C. | A只能是金属元素 | |
| D. | A可能是第二周期的ⅡA族或ⅣA族元素 |
| A. | 0.5 摩尔 | B. | 2 摩尔 | C. | 2.5 摩尔 | D. | 4 摩尔 |
| A. | NaHA溶液的pH一定大于7 | |
| B. | 在Na2A,NaHA两种溶液中,离子种类相同 | |
| C. | 在Na2A,NaHA两种溶液中都有c(OH-)+c(A2-)=c(H2A)+c(H+) | |
| D. | 在溶质的物质的量相等的Na2A,NaHA两种溶液中,阴离子总数相等 |
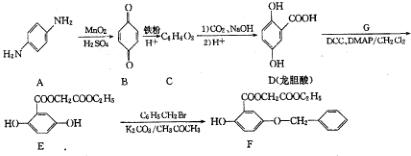
 ;
; ;
;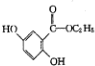 )的一种同分异构体的结构简式
)的一种同分异构体的结构简式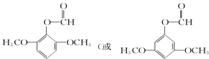 ;
;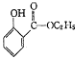 )的合成路线流程图(无机试剂任用),相关信息:
)的合成路线流程图(无机试剂任用),相关信息: .
.
 ;已知甲为二元弱酸,写出甲在水中电离出一个H+的电离方程式H2O2?H++HO2-.
;已知甲为二元弱酸,写出甲在水中电离出一个H+的电离方程式H2O2?H++HO2-.