题目内容
 含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、SO3、Na2SO3、CuSO4、Na2SO4这7种常见的含硫化合物.回答下列问题:
含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、SO3、Na2SO3、CuSO4、Na2SO4这7种常见的含硫化合物.回答下列问题:(1)写出硫元素在周期表中位置
(2)Ba2+有剧毒.某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒.试写出碳酸钡与胃酸(以盐酸表示)反应的离子反应方程式
(3)对于反应2SO2(g)+O2(g)?2SO3(g),当其他条件不变时,压缩容器体积,则生成SO3的速率将
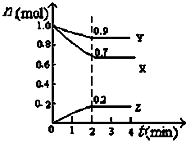
(4)某温度时,在2L密闭容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.由图中的数据分析,该反应的化学方程式为
考点:物质的量或浓度随时间的变化曲线,化学反应速率的影响因素,含硫物质的性质及综合应用
专题:
分析:(1)硫元素属于第16号元素;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水;
(3)增大压强、浓度、升高温度、使用催化剂均加快反应速率;
(4)随反应进行,X、Y物质的量减少,为反应物,Z的物质的量增大,为生成物,根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式,根据v=
计算.
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水;
(3)增大压强、浓度、升高温度、使用催化剂均加快反应速率;
(4)随反应进行,X、Y物质的量减少,为反应物,Z的物质的量增大,为生成物,根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式,根据v=
| △c |
| △t |
解答:
解:(1)硫元素属于第16号元素在周期表中位置为:第三周期,第VIA族;
故答案为:第三周期,第VIA族;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,奇反应的离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;(3)对于反应2SO2(g)+O2(g)?2SO3(g),当其他条件不变时,压缩容器体积,压强增大,则生成SO3的速率将加快,增大O2的浓度时,反应速率将加快,使用V2O5作催化剂时,反应速率将加快,降低温度时,反应速率将减慢,故答案为:加快;加快;加快;减慢;
(4)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,则△n(X):△n(Y):△n(Z)=3:1:2,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X+Y?2Z;
反应开始至2min末,Z的反应速率为:v=
=0.05mol/(L?min),故答案为:3X+Y?2Z;0.05mol/(L?min).
故答案为:第三周期,第VIA族;
(2)碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,奇反应的离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;(3)对于反应2SO2(g)+O2(g)?2SO3(g),当其他条件不变时,压缩容器体积,压强增大,则生成SO3的速率将加快,增大O2的浓度时,反应速率将加快,使用V2O5作催化剂时,反应速率将加快,降低温度时,反应速率将减慢,故答案为:加快;加快;加快;减慢;
(4)由图象可以看出,反应中X、Y的物质的量减少,应为反应物,Z的物质的量增多,应为生成物,当反应进行到2min时,△n(X)=0.3mol,△n(Y)=0.1mol,△n(Z)=0.2mol,则△n(X):△n(Y):△n(Z)=3:1:2,参加反应的物质的物质的量之比等于化学计量数之比,则反应的方程式为:3X+Y?2Z;
反应开始至2min末,Z的反应速率为:v=
| ||
| 2min |
点评:本题考查较综合,涉及物质的量与浓度图象、反应速率的影响因素、物质的性质及元素的位置等,把握物质的性质及反应原理是解题关键,侧重分析与应用能力的考查,题目难度中等.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述错误是( )

| A、1 mol M最多可与5 mol H2(不考虑酯键与氢气加成)反应 |
| B、M可溶于稀NaOH溶液,且加热时发生水解反应 |
| C、1 mol M在浓硫酸存在下可与2 mol CH3COOH发生酯化反应 |
| D、1 mol M可与1 mol HBr(氢溴酸)反应 |
下列物质分别与NaOH的醇溶液共热后,能发生消去反应,且生成物只有一种的是( )
A、 |
B、 |
| C、CH3Cl |
D、 |
下列有机物中含有的杂质(括号内为杂质),可用稀NaOH溶液作试剂并采用分液的方法除去的是( )
| A、苯(溴) |
| B、淀粉(葡萄糖) |
| C、甲苯(苯酚) |
| D、苯甲酸(苯酚) |



