题目内容
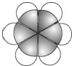
 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )| A、气态氢化物的稳定性:Y>X |
| B、原子半径:W>Z>Y>X |
| C、X、Z、W的气态氢化物溶于水均呈酸性 |
| D、最高价氧化物对应水化物的酸性:Z>W>X |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W均为短周期元素,Y原子的最外层电子数是次外层电子数的3倍,次外层电子数为2,最外层电子数为6,则Y为O元素;由图中的位置可知,X为N元素,Z为S元素,W为Cl元素,据此解答.
解答:
解:X、Y、Z、W均为短周期元素,Y原子的最外层电子数是次外层电子数的3倍,次外层电子数为2,最外层电子数为6,则Y为O元素;由图中的位置可知,X为N元素,Z为S元素,W为Cl元素.
A.非金属性N<O,稳定性NH3<H2O,故A正确;
B.电子层越多,半径越大,同周期从左向右原子半径依次减小,则原子半径为Z>W>X>Y,故B错误;
C.氨气的水溶液呈碱性,故C错误;
D.非金属性W>X>Z,则最高价氧化物对应的水化物的酸性为W>X>Z,故D错误;
故选A.
A.非金属性N<O,稳定性NH3<H2O,故A正确;
B.电子层越多,半径越大,同周期从左向右原子半径依次减小,则原子半径为Z>W>X>Y,故B错误;
C.氨气的水溶液呈碱性,故C错误;
D.非金属性W>X>Z,则最高价氧化物对应的水化物的酸性为W>X>Z,故D错误;
故选A.
点评:本题考查位置结构性质关系,推断元素是解答本题的关键,注意把握元素周期律的递变规律.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
下列说法正确的是( )
| A、使用催化剂一定能使所有的反应提高反应速率 |
| B、中和反应都是放热反应 |
| C、当反应物浓度等于生成物浓度时,可逆反应一定已达到化学平衡状态 |
| D、水力发电是将化学能转化为电能的过程 |
在一定条件下,将64g SO2气体和32g氧气通入密闭容器中生成SO3气体,达到平衡时,共放出热量78.64KJ,已知SO2在此条件下转化率为80%,则下列热化学方程式正确的是( )
A、SO2(g)+
| ||
| B、2SO2(g)+O2(g)?2SO3(g);△H=-196.6KJ?mol-1 | ||
C、SO2(g)+
| ||
| D、2SO2(g)+O2(g)?2SO3(g);△H=+196.6KJ?mol-1 |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3.则下列说法正确的是( )
| A、反应过程中,被氧化与被还原的元素的物质的量之比为2:1 |
| B、NF3是一种无色、无臭的气体,因此NF3在空气中泄漏时不易被察觉 |
| C、一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少空气污染 |
| D、若反应中生成1.0mol HNO3,转移的电子数目为6.02×1023 |
 以下为五种有机物的有关信息,根据表中信息回答问题.
以下为五种有机物的有关信息,根据表中信息回答问题.