题目内容
7.Ⅰ.工业上制取硝酸的主要流程图如图1: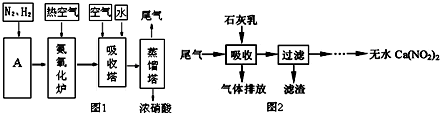
(1)工业合成氨的原料是N2和H2.装置A的名称是合成塔;其中N2可从空气中分离出来,方法是先将空气液化,然后蒸馏或控制N2的沸点加热蒸发即可得到;H2可以水和天然气为原料在催化剂作用下高温制取,其化学方程式为CH4+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO+3H2.
(2)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应:CO(g)+H2O(g)═CO2(g)+H2(g)来实现.已知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于5.8.
Ⅱ.利用石灰乳来除去硝酸工业的尾气(含NO、NO2),既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如图2.已知NO和NO2按1:1通入碱液中生成亚硝酸盐.
(3)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是使尾气中的NO、NO2 被充分吸收;滤渣可循环使用,滤渣的主要成分是Ca(OH)2(填化学式).
(4)该工艺需控制NO 和NO2 物质的量之比接近1:1.若n(NO):n(NO2)>1:1,则会导致排放气体中NO 含量升高;若n(NO):n(NO2)<1:1,则会导致产品Ca(NO2)2 中Ca(NO3)2 含量升高.
分析 (1)工业上采用氨氧化法制硝酸.首先N2和H2在合成塔中合成NH3,然后在氧化炉中将NH3氧化为NO2,在吸收塔中NO2与O2、H2O反应生成HNO3,最后稀HNO3在蒸馏塔中浓缩制得浓硫酸;
(2)分离空气中氮气的方法:先液化空气,然后采用蒸馏或控制氮气的沸点加热蒸发分离出氮气;
(3)工业制硝酸的尾气处理,主要采用碱性石灰乳吸收NO和NO2,滤渣中的石灰乳可回收利用,既经济合理,又绿色环保;
(4)硝酸工业尾气NO、NO2用碱液吸收的主反应为NO+NO2+2OH-=2NO2-+H2O,副反应为2NO2+2OH-=NO2-+NO3-+H2O.要控制NO、NO2的比例为1:1,才能保证主反应完全反应.若NO过量,NO不能得到充分的吸收;若NO2多了,副反应就会生成Ca(NO3)2.
解答 解:(1)N2与H2合成氨是在合成塔中进行的.其中N2的制备,是将空气液化,然后进行蒸馏或者控制N2沸点加热蒸发制得;反应物和条件题干已经给出,只需写出生成物、配平反应方程式为CH4+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO+3H2,
故答案为:合成塔;液化;蒸馏或控制N2的沸点加热蒸发;CH4+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO+3H2;
(2)设c(H2O):c(CO)为X.假设初始c(H2O)为X,则c(CO)为.由CO(g)+H2O(g)═CO2(g)+H2(g)可知,要使CO转化率达到0.8,则平衡时各物质的浓度为c(CO)=0.2; c(H2O)=X-0.8;c(CO2)=0.8;c(H2)=0.8.由平衡常数K=$\frac{0.8×0.8}{(X-0.8)×0.2}=0.64$,可解得X=5.8,
故答案为:5.8;
(3)使用吸收塔的好处就在于,增大尾气与吸收液之间接触的面积,从而提高尾气的吸收率.滤渣中可回收利用的是过量的石灰乳,也就是Ca(OH)2.
故答案为:使尾气中的NO、NO2 被充分吸收;Ca(OH)2;
(4)硝酸工业尾气NO、NO2一般用碱液吸收,主反应为:NO+NO2+2OH-=2NO2-+H2O,副反应为:2NO2+2OH-=NO2-+NO3-+H2O.若n(NO):n(NO2)>1:1,则一氧化氮过量,排放气体中NO含量升高;若n(NO):n(NO2)<1:1,则二氧化氮过量,二氧化氮与石灰乳反应生成Ca(NO3)2,
故答案为:排放气体中NO含量升高;产品Ca(NO2)2中Ca(NO3)2含量升高.
点评 本题主要考察硝酸工业生产中尾气的处理问题,契合我国当前绿色生产的理念,此类问题近期考察频率很高.

 互动英语系列答案
互动英语系列答案| A. | 鸡蛋白溶液中分散质的微粒直径在1~100 nm之间 | |
| B. | 当日光从窗隙射入暗室时,可观察到一束光线 | |
| C. | 向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 | |
| D. | 在河流入海处易形成沙洲 |
| A. | HClO 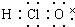 | B. | OH- 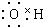 | C. | HCl  | D. | Na2O2 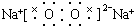 |
| A. | N2 | B. | N2O | C. | N2O4 | D. | N2O5 |
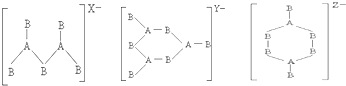
由此可知三种离子的电荷数X、Y、Z分别为( )
| A. | 2,3,4 | B. | 4,3,2 | C. | 4,2,3 | D. | 3,2,4 |
| A. | 糖类、油脂和蛋白质都能发生水解反应 | |
| B. | 淀粉、纤维素、蛋白质都属于天然有机高分子化合物 | |
| C. | 采用多次盐析和溶解,可以分离提纯蛋白质 | |
| D. | 一般情况下,天然油脂都可以发生加成反应 |
| A. | 氨极易溶于水 | B. | 铵离子不能独立存在 | ||
| C. | 常温下氨是气态物质 | D. | 氮原子不能形成阳离子 |