题目内容
依据事实,用化学用语填空:
①1mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46kJ.该反应的热化学方程式 .
②用离子方程式表示氯化铵溶液的酸碱性: .
③用离子方程式表示向碳酸镁沉淀中加入NaOH溶液后的沉淀转化: .
①1mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46kJ.该反应的热化学方程式
②用离子方程式表示氯化铵溶液的酸碱性:
③用离子方程式表示向碳酸镁沉淀中加入NaOH溶液后的沉淀转化:
考点:离子方程式的书写,热化学方程式
专题:
分析:①1mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46kJ,则3mol气体参加反应放出46kJ×3=138kJ热量;
②氯化铵溶液,铵根离子水解显酸性;
③碳酸镁沉淀中加入NaOH溶液,生成更难溶的氢氧化镁沉淀.
②氯化铵溶液,铵根离子水解显酸性;
③碳酸镁沉淀中加入NaOH溶液,生成更难溶的氢氧化镁沉淀.
解答:
解:①1mol NO2气体与水完全反应生成硝酸溶液和NO气体,放出热量46kJ,则3mol气体参加反应放出46kJ×3=138kJ热量,则热化学方程式为3NO2(g)+H2O(l)═2HNO3(aq)+NO(g)△H=-138kJ/mol,故答案为:3NO2(g)+H2O(l)═2HNO3(aq)+NO(g)△H=-138kJ/mol;
②氯化铵溶液,铵根离子水解显酸性,水解离子反应为NH4++H2O?NH3?H2O+H+,故答案为:NH4++H2O?NH3?H2O+H+;
③碳酸镁沉淀中加入NaOH溶液,生成更难溶的氢氧化镁沉淀,离子反应为MgCO3+2OH-═Mg(OH)2+CO32-,故答案为:MgCO3+2OH-═Mg(OH)2+CO32-.
②氯化铵溶液,铵根离子水解显酸性,水解离子反应为NH4++H2O?NH3?H2O+H+,故答案为:NH4++H2O?NH3?H2O+H+;
③碳酸镁沉淀中加入NaOH溶液,生成更难溶的氢氧化镁沉淀,离子反应为MgCO3+2OH-═Mg(OH)2+CO32-,故答案为:MgCO3+2OH-═Mg(OH)2+CO32-.
点评:本题考查离子反应的书写,为高考常见题型,把握热化学方程式、盐类水解、沉淀转化等为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14 6 |
14 6 |
| A、质子数为14 |
| B、中子数为6 |
| C、电子数为6 |
| D、质量数为8 |
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、1 mol Cl2与足量Fe反应,转移的电子数为3NA |
| B、常温常压下,14g氮气中含有 NA个原子 |
| C、标准状况下,22.4L水中含有的原子数为3NA |
| D、在25℃、101 kPa时,22.4 L氢气中含有NA个氢分子 |
下列方程式书写不正确的是( )
| A、NaHS水解:HS-+H2O?H2S+OH- |
| B、氢氧化钡溶于水电离:Ba(OH)2═Ba2++2OH- |
| C、醋酸溶于水电离:CH3COOH?CH3COO-+H+ |
| D、碳酸钠水解:CO32-+2H2O?2OH-+H2CO3 |
下列关于铜电极的叙述中不正确的是( )
| A、铜锌原电池中铜是正极 |
| B、在镀件上镀铜时可以用金属铜作阳极 |
| C、用电解法精炼粗铜时粗铜作阴极 |
| D、镀铜的铁器,若发生缺损易形成以铜为正极的原电池 |
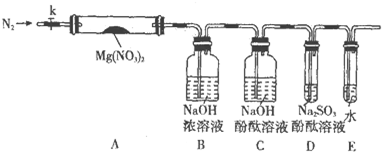 固体硝酸盐加热易分解且产物较复杂.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下:
固体硝酸盐加热易分解且产物较复杂.已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应方程式如下: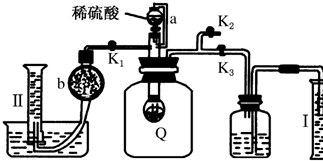 为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.
为测定保存在干燥环境中已部分变质的过氧化钠样品(只有一种杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开漏斗的活塞,将稀硫酸滴入气球中.