题目内容
设NA为阿佛加德罗常数的值,下列说法正确的是( )
| A、25℃时,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、在标准状况下,2.24 L CH2Cl2含有σ键的数目为0.4NA |
| C、某密闭容器盛有0.1molN2与0.3molH2,在一定条件下充分反应生成NH3,转移的电子数为0.6NA |
| D、向沸水中逐滴加入100 mL 0.1 mol/L饱和FeCl3溶液,形成的胶粒数小于0.01NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉氢氧化钠溶液的体积;
B.标准状况下,CH2Cl2为液体;
C.合成氨的反应是可逆反应不能进行彻底;
D.氢氧化铁胶粒为氢氧化铁的聚集体.
B.标准状况下,CH2Cl2为液体;
C.合成氨的反应是可逆反应不能进行彻底;
D.氢氧化铁胶粒为氢氧化铁的聚集体.
解答:
解:A.没有告诉PH=13的NaOH溶液的体积,无法计算氢氧化钠的物质的量,故A错误;
B.标准状况下,CH2Cl2为液体,2.24 L CH2Cl2物质的量不是0.1mol,故B错误;
C.在密闭容器中,0.1molN2与0.3molH2在一定条件下充分反应,反应是可逆反应,不能进行完全,生成氨气的分子数小于0.6NA,故C错误;
D.由于氢氧化铁胶粒为氢氧化铁的聚集体,形成的胶粒数小于0.01NA,故D正确.
故选D.
B.标准状况下,CH2Cl2为液体,2.24 L CH2Cl2物质的量不是0.1mol,故B错误;
C.在密闭容器中,0.1molN2与0.3molH2在一定条件下充分反应,反应是可逆反应,不能进行完全,生成氨气的分子数小于0.6NA,故C错误;
D.由于氢氧化铁胶粒为氢氧化铁的聚集体,形成的胶粒数小于0.01NA,故D正确.
故选D.
点评:本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
对反应xR2++yH++O2=mR3++nH2O的离子方程式中,对m和R3+判断正确的是( )
| A、m=4,R3+是氧化产物 | ||
| B、m=y,R3+是还原产物 | ||
| C、m=2,R3+是氧化产物 | ||
D、m=
|
将如图中所示实验装置的K闭合,下列判断正确的是( )
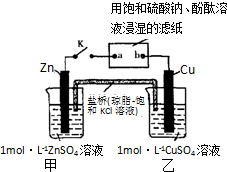

| A、电子沿Zn→a→b→Cu路径流动 |
| B、Cu电极上发生氧化反应 |
| C、甲池与乙池中的溶液互换,闭合K仍有电流产生 |
| D、片刻后可观察到滤纸a点变红色 |
下列叙述正确的是( )
| A、焓变是一个与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| B、增大压强是通过提高活化分子的百分数来提高反应速率 |
| C、氮的固定只有在高温、高压、催化剂的条件下才能实现 |
| D、水煤气是可再生能源 |
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- |
| B、Al2O3与NaOH溶液反应 Al2O3+2OH-═2[Al(OH)4]- |
| C、FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢 2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温常压下,18克H2O含有2NA个氢原子 |
| B、1mol的Cl2与足量的NaOH溶液反应转移的电子数为2NA |
| C、1mol苯分子中含有的碳碳双键数为3 NA |
| D、5mol/L的Na2CO3溶液中含有的CO32-数目小于0.5 NA |
在酸性溶液中,下列各组离子能大量共存的是( )
| A、Cl-、HCO3-、K+、SO42- |
| B、OH-、Cl-、Na+、Mg2+ |
| C、Fe3+、Na+、SO32-、I- |
| D、Na+、Cl-、I-、SO42- |
下列关于晶体的叙述错误的是( )
| A、分子晶体中可能不含共价键 |
| B、原子晶体中只存在共价键 |
| C、离子晶体中一定含有离子键 |
| D、分子晶体中可能含有离子键 |