题目内容
在下列实验中,不能达到目的是( )
| A、Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S |
| B、用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜、镁的金属活动性强弱 |
| C、进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱 |
| D、测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱 |
考点:化学实验方案的评价
专题:
分析:A.Cl得电子能力比S的强;
B.石墨作电极,阴极上铜离子先得到电子;
C.H2O和H2S的热分解实验中,水稳定;
D.NaCl和NaF溶液的pH,NaCl的pH=7,NaF的pH>7,则HCl为强酸、HF为弱酸.
B.石墨作电极,阴极上铜离子先得到电子;
C.H2O和H2S的热分解实验中,水稳定;
D.NaCl和NaF溶液的pH,NaCl的pH=7,NaF的pH>7,则HCl为强酸、HF为弱酸.
解答:
解:A.Cl得电子能力比S的强,则Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,可比较非金属性:Cl>S,故A正确;
B.石墨作电极,阴极上铜离子先得到电子,则氧化性铜离子大于镁离子,可比较铜、镁的金属活动性强弱,故B正确;
C.H2O和H2S的热分解实验中,水稳定,则非金属性O>S,故C正确;
D.NaCl和NaF溶液的pH,NaCl的pH=7,NaF的pH>7,则HCl为强酸、HF为弱酸,但不能比较非金属性,比较角度不合理,故D错误;
故选D.
B.石墨作电极,阴极上铜离子先得到电子,则氧化性铜离子大于镁离子,可比较铜、镁的金属活动性强弱,故B正确;
C.H2O和H2S的热分解实验中,水稳定,则非金属性O>S,故C正确;
D.NaCl和NaF溶液的pH,NaCl的pH=7,NaF的pH>7,则HCl为强酸、HF为弱酸,但不能比较非金属性,比较角度不合理,故D错误;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,把握氧化还原反应、电解原理、非金属性的比较方法等为解答的关键,侧重实验评价及化学反应原理的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、常温下,铜与氧气很难反应,因为铜和氧气的反应是吸热反应 |
| B、金属锂在常温和加热情况下与氧气反应的产物不同 |
| C、焰色反应实验中的铂丝应用稀盐酸洗涤 |
| D、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
 已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应方程式为:
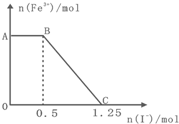
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液(假设I-与KMnO4反应的氧化产物为I2),混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 | ||||
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2通电 | ||||
| C、根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol | ||||
D、以Pt为电极材料电解C点的溶液,总反应式为2H2O
|
某烃1mol 最多能和2molHBr 加成反应,其所得的产物又能跟8molBr2 发生取代反应,最后得到一种只含碳、溴两种元素的化合物,则原烃为( )
| A、C4H6 |
| B、C3H4 |
| C、C3H6 |
| D、C2H2 |
下列物质中,属于电解质的是( )
| A、氯化钾溶液 | B、澄清石灰水 |
| C、酒精 | D、氯化钠晶体 |
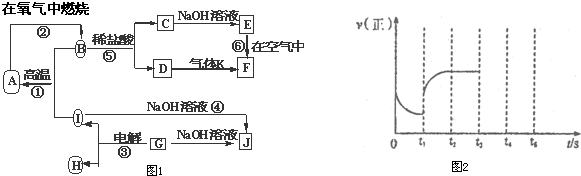
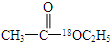 .写出有关反应的化学方程式.
.写出有关反应的化学方程式.