题目内容
下列离子方程式不正确的是
A.0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:
HSO3-+ClO-=SO42-+Cl-+H+
B.氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O
C.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:
Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO
D.NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全:NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O
A
【解析】
试题分析:A、0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合发生氧化还原反应,由于次氯酸钠过量,所以溶液中还有次氯酸生成,离子方程式应为HSO3-+2ClO-=SO42-+Cl-+HClO,错误;B、氢氧化铁溶于氢碘酸中,发生氧化还原反应生成亚铁离子和碘,符合离子方程式的书写,正确;C、次氯酸根离子与铁离子发生双水解生成氢氧化铁和次氯酸,正确;D、NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全时氢氧根离子与氢离子反应生成水铵根离子与氢氧根离子反应生成一水合氨,正确,答案选A。
考点:考查离子方程式的判断

练习册系列答案
相关题目
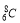 B.甲烷分子的比例模型:
B.甲烷分子的比例模型:
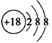
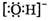 D.氯离子的结构示意图:
D.氯离子的结构示意图: