题目内容
4.下列离子方程式正确的是( )| A. | 碳酸氢铵溶液与足量氢氧化钠溶液混合后加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 将少量氯化铁溶液滴入硫化钠溶液中:2Fe3++S2-═2Fe2++S↓ | |
| C. | 向Fe(NO3) 2稀溶液中加入盐酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| D. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
分析 A.漏掉碳酸氢根离子与氢氧根离子的反应;
B.反应生成FeS和S;
C.硝酸根离子在酸性环境下能够氧化二价铁离子生成三价铁离子;
D.二氧化碳过量,反应生成碳酸氢钙和次氯酸.
解答 解:A.碳酸氢铵溶液与足量氢氧化钠溶液混合后加热,离子方程式:HCO3-+NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+2H2O+CO32-,故A错误;
B.将少量氯化铁溶液滴入硫化钠溶液中的离子反应为2Fe3++3S2-=2FeS+S↓,故B错误;
C.向Fe(NO3) 2稀溶液中加入盐酸,离子方程式:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑,故C正确;
D.次氯酸钙溶液中通入过量二氧化碳,离子方程式:ClO-+H2O+CO2=HCO3-+HClO,故D错误;
故选:C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.将0.1mol两种气态烃(其中一种为炔烃)组成的混合气体完全燃烧后得3.36L(标况)CO2和3.6g H2O.则这两种烃的物质的量之比说法正确的是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 无法计算 |
15.某电池总反应为 2Fe3++Cu═2Fe2++Cu2+,不能实现该反应的原电池是( )
| A. | 电极材料 Fe、Cu,电解质溶液 FeCl3 溶液 | |
| B. | 电极材料石墨、Cu,电解质溶液 Fe2(SO4)3溶液 | |
| C. | 电极材料 Pt、Cu,电解质溶液 FeCl3溶液 | |
| D. | 电极材料 Ag、Cu,电解质溶液 Fe2(SO4)3溶液 |
12.己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述不正确的是( )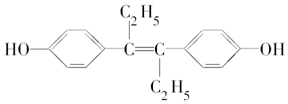

| A. | 可以使溴水褪色 | |
| B. | 该物质能发生氧化反应 | |
| C. | 1 mol该有机物可以与5 mol Br2发生反应 | |
| D. | 可与NaOH和NaHCO3溶液发生反应 |
19.用下图所示实验装置进行相应实验,能达到实验目的是( )
| A. | .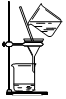 装置可用于除去乙醇中的溴苯 | |
| B. | .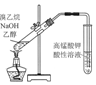 用图所示装置检验溴乙烷与NaOH醇溶液共热产生的C2H4 | |
| C. | .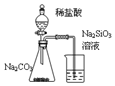 装置可证明非金属性Cl>C>Si | |
| D. | 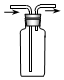 装置可用于收集O2 |
9.同主族常见的三种元素 X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4,下列判断不正确的是( )
| A. | Y 单质可以在海水中提取 | B. | 单质氧化性:Y>Z | ||
| C. | 气态氢化物稳定性:HX<HZ | D. | 离子半径:X->Y- |
3.X、Y、Z、W是原子序数依次增大的四种短周期元素,p、q、r是Y分别与X、Z、W形成的二元化合物,p与q反应生成盐及一种单质Y2,其中该盐与盐酸反应有气体生成,r与BaCl2溶液反应生成不溶于盐酸的白色沉淀.下列说法错误的是( )
| A. | 简单离子半径:W>Y>Z | |
| B. | 最高价氧化物对应水化物的酸性:W>X | |
| C. | 单质熔点:X>W>Y | |
| D. | q与p、r的化学键种类完全不同 |
4.有机物X的结构简式如图,下列说法正确的是( )
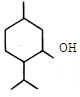

| A. | X分子式为C10H20O,它是环己醇的同系物 | |
| B. | X分子环上的一氯取代物只有三种 | |
| C. | X分子中至少有12个原子在同一平面上 | |
| D. | 在一定条件下,X能发生取代反应、氧化反应、聚合反应 |