题目内容
6.在浓盐酸中HNO2与SnCl2反应的离子方程式为3SnCl2+12Cl-+2HNO2+6H+═N2+3SnClxy-+4H2O,关于该反应的说法都正确的是( )①氧化剂是HNO2;②还原性:Cl->N2;③每生成2.8gN2,还原剂失去的电子为0.6mol;④x为6,y为2;⑤SnClx-是氧化产物.
| A. | ①③ | B. | ①③④⑤ | C. | ①②③④ | D. | ①④⑤ |
分析 3SnCl2+12Cl-+2HNO2+6H+═N2+3SnClxy-+4H2O,由电荷守恒可知,y为2,由原子守恒可知x=6,Sn元素的化合价升高,N元素的化合价降低,结合氧化还原反应中还原剂的还原性大于还原产物的还原性及氧化剂的氧化性大于氧化产物的氧化性来解答.
解答 解:①N元素的化合价降低,则氧化剂是HNO2,故正确;
②Cl元素的化合价不变,则该反应中不能判断Cl-、N2还原性强弱,故错误;
③每生成2.8g N2,得到电子为$\frac{2.8g}{28g/mol}$×2×(3-0)=0.6mol,由电子守恒可知还原剂失去的电子为0.6mol,故正确;
④由原子守恒可知x为6,由电荷守恒可知y为2,故正确;
⑤Sn元素失去电子被氧化,则SnClxy-是氧化产物,故正确;
故选B.
点评 本题考查了氧化还原反应,为高频考点,明确元素化合价变化是解本题关键,注意守恒法的应用及氧化还原反应基本概念,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
10.能在水溶液中大量共存的一组离子是( )
| A. | H+、Fe3+、I-、SO${\;}_{4}^{2-}$ | B. | OH-、Na+、HCO${\;}_{3}^{-}$、Cl- | ||
| C. | K+、Ca2+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$ | D. | K+、Na+、OH-、AlO${\;}_{2}^{-}$ |
11.粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是燃煤发电过程中产生的废渣,粉煤灰的综合利用具有很大的价值.
Ⅰ.研究人员通过实验对粉煤灰中铝和铁元素的分离工艺进行了研究.
(1)以硫酸溶液分解粉煤灰,使其中的铝、铁元素溶出,过滤实现初步分离.
①写出硫酸溶液与Fe2O3反应的离子方程式6H++Fe2O3=2Fe3++3H2O.
②初步分离得到的滤渣主要成分是SiO2.
(2)向(1)分离所得的滤液中加入还原剂使Fe3+转化为Fe2+,结合表分析其原因Fe(OH)3和Al(OH)3沉淀的pH相近,不易通过沉淀分离.
(3)使用碱性较弱的氨水为pH调节剂,进行分离实验.
①氨水使滤液中铝离子沉淀的离子方程式为3NH3•H2O+Al3+=Al(OH)3+3NH4+.
②反应终点的pH对铝和铁分离效果的影响如图1.根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是略小于5,选择该范围的理由是铝元素沉淀较多,铁元素还没有开始大量的沉淀.

Ⅱ.NH4HSO4和H2SO4按物质的量比1:1混合配制成浸取液,220℃时,可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4)2],然后分离、煅烧获得纯Al2O3.
已知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g.
②280℃时分解.
(1)依据资料可知,将硫酸铝铵与其他溶质分离的方法是冷却、结晶.
(2)煅烧NH4Al(SO4)2同时得到混合气体(NH3、N2、SO2、SO3、H2O).若16mol混合气体按图2装置被完全吸收制得浸取液,请将图2中试剂及其物质的量补充完整.
Ⅰ.研究人员通过实验对粉煤灰中铝和铁元素的分离工艺进行了研究.
(1)以硫酸溶液分解粉煤灰,使其中的铝、铁元素溶出,过滤实现初步分离.
①写出硫酸溶液与Fe2O3反应的离子方程式6H++Fe2O3=2Fe3++3H2O.
②初步分离得到的滤渣主要成分是SiO2.
(2)向(1)分离所得的滤液中加入还原剂使Fe3+转化为Fe2+,结合表分析其原因Fe(OH)3和Al(OH)3沉淀的pH相近,不易通过沉淀分离.
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 沉淀区间(pH) | 7.06~8.95 | 1.94~3.20 | 3.69~4.8 |
①氨水使滤液中铝离子沉淀的离子方程式为3NH3•H2O+Al3+=Al(OH)3+3NH4+.
②反应终点的pH对铝和铁分离效果的影响如图1.根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是略小于5,选择该范围的理由是铝元素沉淀较多,铁元素还没有开始大量的沉淀.

Ⅱ.NH4HSO4和H2SO4按物质的量比1:1混合配制成浸取液,220℃时,可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4)2],然后分离、煅烧获得纯Al2O3.
已知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g.
②280℃时分解.
(1)依据资料可知,将硫酸铝铵与其他溶质分离的方法是冷却、结晶.
(2)煅烧NH4Al(SO4)2同时得到混合气体(NH3、N2、SO2、SO3、H2O).若16mol混合气体按图2装置被完全吸收制得浸取液,请将图2中试剂及其物质的量补充完整.
8.下列关于有机物的说法正确的是( )
| A. | 甲烷、乙烯和苯在工业上都可以通过石油分馏得到 | |
| B. | 苯和乙烯都可使溴的四氯化碳溶液褪色 | |
| C. | 甲烷、乙烯、乙醇都能发生氧化反应 | |
| D. | 汽油、柴油属于烃,植物油属于高分子化合物 |
1.以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的是( )
| A. | 现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3:2:1 | |
| B. | n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为$\frac{35.5m}{n}$ | |
| C. | 标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 | |
| D. | 5.6 g CO和22.4 L CO2中含有的碳原子数一定相等 |
18.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 叙述I | 叙述II |
| A.NH4Cl受热易分解 | 可用加热法除去I2中的NH4Cl |
| B.往氯化钙溶液中通入足量的CO2 先有白色沉淀生成,后沉淀溶解 | CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C.水玻璃具有黏性 | 盛装烧碱溶液的试剂瓶不能用玻璃塞 |
| D.利用丁达尔现象区分氢氧化铁胶体和浓的氯化铁溶液 | 往氢氧化钠溶液中滴加饱和氯化铁溶液,加热至红褐色制得胶体 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关实验装置(夹持和尾气处理装置已省略)进行的相应实验,不能达到实验目的是( )
| A. | 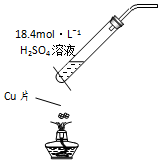 用图装置制取SO2 | |
| B. | 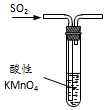 图装置中溶液的颜色变浅,说明SO2具有漂白性 | |
| C. | 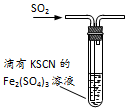 图装置中溶液的颜色变浅,说明SO2具有还原性 | |
| D. |  图装置中产生淡黄色沉淀,说明SO2或H2SO3具有氧化性 |
3.下列物质属于电解质的是( )
| A. | 稀盐酸 | B. | 二氧化碳 | C. | 酒精 | D. | 硫酸钡 |