题目内容
温度为T1时,向容积不变的密闭容器中通入2mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.反应一段时间后,将反应体系的温度瞬间升高至T2,此后开始连续测定体系中SO2的百分含量(SO2%),并作出SO2的百分含量随时间(t)的变化关系图,示意图中哪一个不可能与实验结果相符?( )
A、 |
B、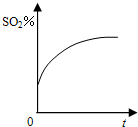 |
C、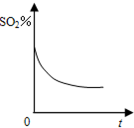 |
D、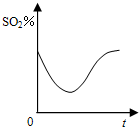 |
考点:产物的百分含量随浓度、时间的变化曲线
专题:图示题,化学平衡专题
分析:将反应体系的温度瞬间升高至T2,可能没达到平衡状态,然后向正向进行建立化学平衡的阶段,该过程中,二氧化硫的百分含量是逐渐减小的;可能达到平衡状态,再升高温度,会使已经建立的化学平衡逆向移动,二氧化硫的百分含量会逐渐升高;升温瞬间,可能达到平衡状态,二氧化硫的百分含量的变化不随着时间的变化而变化,以此来回答.
解答:
解:温度为T1时,向容积不变的密闭容器中通入2mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g),开始阶段是平衡的建立过程,反应正向进行,二氧化硫的百分含量逐渐减小,达到平衡以后,升高温度,会使得化学平衡逆向移动,二氧化硫的百分含量会逐渐升高,直到达到新的化学平衡状态.
A、将反应体系的温度瞬间升高至T2,可能达到平衡状态,二氧化硫的百分含量的变化不随着时间的变化而变化,故A不选;
B、将反应体系的温度瞬间升高至T2,可能达到平衡状态,再升高温度,会使已经建立的化学平衡逆向移动,二氧化硫的百分含量会逐渐升高,可能,故B不选;
C、将反应体系的温度瞬间升高至T2,可能没达到平衡状态,然后向正向进行建立化学平衡的阶段,该过程中,二氧化硫的百分含量是逐渐减小的,故C不选;
D、整个阶段,二氧化硫的百分含量可能减小,或不变,或升高温度逐渐增大,而先减小后增大不可能,故D选.
故选D.
A、将反应体系的温度瞬间升高至T2,可能达到平衡状态,二氧化硫的百分含量的变化不随着时间的变化而变化,故A不选;
B、将反应体系的温度瞬间升高至T2,可能达到平衡状态,再升高温度,会使已经建立的化学平衡逆向移动,二氧化硫的百分含量会逐渐升高,可能,故B不选;
C、将反应体系的温度瞬间升高至T2,可能没达到平衡状态,然后向正向进行建立化学平衡的阶段,该过程中,二氧化硫的百分含量是逐渐减小的,故C不选;
D、整个阶段,二氧化硫的百分含量可能减小,或不变,或升高温度逐渐增大,而先减小后增大不可能,故D选.
故选D.
点评:本题涉及化学平衡的建立以及化学平衡的移动方向等方面的知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列表达式错误的是( )
A、甲烷的电子式: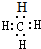 |
B、氮原子的L层电子的电子排布图 |
| C、硫离子的核外电子排布式1s22s22p63s23p4 |
| D、根据价电子对互斥理论,H3O+的空间构型为三角锥形 |
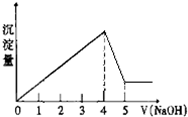 有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
将苯与溴水混合,充分振荡后静置,用分液漏斗分离出上层液体放置于一试管中,若向其中加入一种试剂,可发生反应并产生白雾,这种试剂可以是( )
| A、亚硫酸钠 | B、溴化铁 |
| C、锌粉 | D、铁粉 |
水质检验中,测定水的硬度时,用到氨-氯化氨(NH3-NH4Cl)缓冲溶液,控制溶液在pH=10左右.则关于该缓冲溶液的说法不正确的是( )
| A、将缓冲溶液加水稀释时,pH一定会减小 |
| B、将缓冲溶液升温,pH一定没有变化 |
| C、在缓冲溶液中,水的电离受到抑制 |
| D、在缓冲溶液中,一定有c(NH+4)>c(Cl-) |
我国古代“药金”的冶炼方法是:将炉甘石(ZnCO3)和赤铜矿(Cu2O)与木炭按一定的比例混合后加热至800℃,即可炼出闪烁似金子般光泽的“药金”.下列叙述正确的是( )
| A、“药金”实质上是铜锌合金 |
| B、冶炼炉中炉甘石直接被木炭还原为锌 |
| C、用王水可区别黄金和“药金” |
| D、用火焰灼烧不能区别黄金和药金 |
用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A、常温下,1 L0.1mol/LNa2CO3溶液中,含有阴离子的总数小于0.1 NA |
| B、常温常压下,Na2O2与足量H2O反应,共生成0.2mol O2,转移电子的数目为0.4NA |
| C、5.6 g铁和6.4 g铜分别与0.1 mol氯气完全反应,转移的电子数相等 |
| D、84 gNaHCO3与MgCO3的混合物中所含氧原子数目一定为3NA |
下列有关四种治疗禽流感药物的说法不正确的是( )
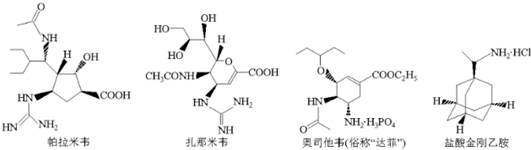

| A、帕拉米韦的分子式为C15H27N4O4 |
| B、扎那米韦与帕拉米韦的钠盐可用新制Cu(OH)2悬浊液鉴别 |
| C、1mol达菲最多能与5molNaOH反应 |
| D、盐酸金刚乙胺六元环上的一个氢原子被氯原子取代,所得一氯代物有三种 |
