题目内容
已知强酸和强碱在稀溶液中发生中和反应生成1molH2O(l)时放出57.30kJ热量,用500mL0.60mol/L
H2SO4溶液与200mL5mol/LNaOH溶液完全反应,放出的热量是( )
H2SO4溶液与200mL5mol/LNaOH溶液完全反应,放出的热量是( )
| A、68.76kJ |
| B、57.30 kJ |
| C、34.38kJ |
| D、17.19 kJ |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:已知中和热的数值,500mL0.60mol/LH2SO4溶液所含氢离子物质的量为0.6mol,200mL5mol/LNaOH溶液含氢氧根离子1.0mol,计算生成0.6mol水时放热多少即可解答.
解答:
解:500mL0.60mol/LH2SO4溶液所含氢离子物质的量为0.6mol,200mL5mol/LNaOH溶液含氢氧根离子1.0mol,生成0.6mol水,生成1mol水时放热57.30KJ,则生成0.6mol水时放热0.6mol×57.30KJ/mol=34.38KJ.
故选:C.
故选:C.
点评:本题主要考查中和热的相关计算,注意过量问题,两种物质反应时若有一种过量,按量少的计算,题目难度不大.

练习册系列答案
相关题目
某实验需2mol/L的Na2CO3溶液950mL,为此配制该溶液时应选用的容量瓶规格和需称取Na2CO3的质量分别是( )
| A、950 mL、201.4 g |
| B、1000 mL、212 g |
| C、任意规格、201.4 g |
| D、1000 mL、201.4 g |
化学与生产、生活、社会密切相关.下列说法中不正确的是( )
| A、“硫黄姜”又黄又亮,可能是在用硫黄熏制的过程中产生的SO2所致 |
| B、天然纤维和人造纤维的主要成分都是纤维素 |
| C、发泡塑料饭盒主要材质是高分子材料,不适于盛放含油较多的食品 |
| D、NaHCO3能与酸反应,因此食品工业用小苏打做焙制糕点的膨松剂 |
分子式为C5H12O2的二元醇,有多种同分异构体,其中主链上碳原子数为3的同分异构体数目为m,主链上碳原子数为4的同分异构体数目为n,则m、n是(一个C上不能连两个-OH)( )
| A、1、6 | B、2、7 |
| C、2、6 | D、1、7 |
已知NH4Ac溶液呈中性,一种c(H+)=10-3mol/L的酸a和pH=11的氨水b以等体积混合后,溶液呈碱性,关于酸a说法正确的是( )
| A、酸a的浓度可能大于b |
| B、酸a的浓度可能等于b |
| C、酸a的酸性比醋酸弱 |
| D、酸a可能是强酸可能是弱酸 |
如图所示,关于该装置的下列叙述中,不正确的是( )
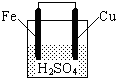

| A、铁棒是负极,发生氧化反应 |
| B、铜棒上有气体放出 |
| C、稀硫酸的pH值不断减小 |
| D、电池总反应方程式可表示为:Fe+2H+=Fe2++H2↑ |
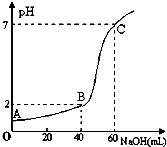 常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示.下列叙述正确的是( )| A、所用HCl的浓度是0.09mol?L-1,NaOH溶液浓度为0.03mol?L-1 |
| B、在B点,溶液中离子浓度关系为:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、A、B、C三点水的电离程度大小依次为:A>B>C |
| D、滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低 |