题目内容
9.下列有关分散系的叙述中不正确的是( )| A. | 胶体分散质粒子较大,不能透过滤纸 | |
| B. | 液态分散系根据分散质粒子大小分为溶液、胶体和浊液三类 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 纳米材料分散到液体分散剂中的分散系属于胶体 |
分析 A.胶粒能透过滤纸;
B.根据分散质微粒的大小可以将混合物进行分类;
C.胶体有丁达尔效应,溶液没有丁达尔效应;
D.纳米材料的直径为1~100 nm之间.
解答 解:A.溶液和胶粒都能透过滤纸,故A错误;
B.根据分散质微粒直径的大小,可以将分散系分为胶体、浊液和溶液三大类,故B正确;
C.胶体有丁达尔效应,溶液没有,故利用丁达尔效应可以区分溶液和胶体,故C正确;
D.纳米材料的直径为1~100 nm之间,分散到液体分散剂中的分散系属于胶体,故D正确.
故选A.
点评 本题考查物质的分类和胶体的性质,注意分类的依据和标准,题目较基础,难度不大.

练习册系列答案
相关题目
19.氢气在氯气中燃烧时发出苍白色火焰,在反应过程中,破坏1mol氢气中的化学键消耗的能量为a kJ,破坏1mol氯气中的化学键消耗的能量为b kJ,形成1mol HCl中的化学键释放的能量为c kJ,下列关系中正确的是( )
| A. | b>c | B. | a+b>2c | C. | a+b<c | D. | a+b<2c |
20.X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示,这四种元素原子的最外层电子数之和为20,下列判断正确的是( )
| W | X | Y |
| Z |
| A. | 四种元素的原子半径:r(Z)>r(X)>r(Y)>r(W) | |
| B. | 四种元素形成的单质最多有6种 | |
| C. | X与Y形成的气态化合物超过两种 | |
| D. | 四种元素中,Z的最高价氧化物对应的水化物酸性最强 |
17.“胃舒平”的主要成分是氢氧化铝,同时含有三硅酸镁(Mg2Si3O8•nH2O)等化合物.下列叙述中错误的是( )
| A. | 镁元素基态原子的核外电子排布式是:1s22s22p63s2 | |
| B. | 铝元素原子核外共有5种不同运动状态的电子 | |
| C. | 钠元素离子半径比铝离子半径大 | |
| D. | 金属铝与钠的最高价氧化物的水化物溶液发生反应的离子方程式为2Al+2OH-+2H2O═2AlO${\;}_{2}^{-}$+3H2↑ |
4.化学与社会发展以及人们生活质量提高有密切的关系.下列各项叙述中不正确的是( )
| A. | 日常生活中的陶瓷、水泥、玻璃等是使用量最大的无机非金属材料 | |
| B. | 制饭勺、高压锅等的不锈钢是合金.合金有许多优良的性能,如熔点比成分金属高 | |
| C. | 防止或减少雾霾形成的措施之一是减少煤的燃烧和机动车的使用 | |
| D. | 食品干燥剂应无毒、无味、无腐蚀性及环境友好,硅胶可用作食品干燥剂 |
14.下列关于硅元素及其化合物的有关说法不正确的是( )
| A. | SiO2是水晶、玛瑙的主要成分,也是制造光导纤维的原料 | |
| B. | SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物 | |
| C. | 盛放NaOH溶液的试剂用橡皮塞,而不用玻璃塞 | |
| D. | Si是良好的半导体材料,是将太阳能转换为电能的常用材料 |
19.如图是某些实验的部分装置,其中能达到实验目的是( )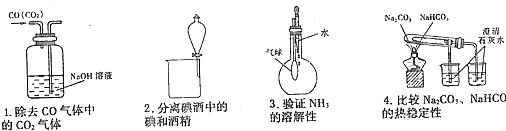

| A. | 1和2 | B. | 3和4 | C. | 1和4 | D. | 全部 |