题目内容
甘油的用途很广,大量用来制造硝化甘油,硝化甘油是甘油与浓硝酸发生酯化反应(在浓硫酸条件下)生成的三硝酸甘油酯.硝化甘油是制备炸药的原料,在医疗上又是心脏病的急救药.试写出以油脂(主要成分是硬脂酸甘油酯)、氨气、空气、水和氢氧化钠为原料制取硝化甘油的化学方程式.
①油脂: ;
②氨气: ;
③空气: ;
④水: ;
⑤氢氧化钠: .
①油脂:
②氨气:
③空气:
④水:
⑤氢氧化钠:
考点:有机物的合成,油脂的性质、组成与结构
专题:有机化合物的获得与应用
分析:以油脂(主要成分是硬脂酸甘油酯)、氨气、空气、水和氢氧化钠为原料制取硝化甘油,根据工业制硝酸的方法,可以先将氨气氧化得一氧化氮,再氧化得二氧化氮,再与水反应得硝酸,将油脂在碱性条件下水解得甘油,将甘油与硝酸在浓硫酸的作用下可得硝化甘油,据此答题;
解答:
解:以油脂(主要成分是硬脂酸甘油酯)、氨气、空气、水和氢氧化钠为原料制取硝化甘油,根据工业制硝酸的方法,可以先将氨气氧化得一氧化氮,再氧化得二氧化氮,再与水反应得硝酸,将油脂在碱性条件下水解得甘油,将甘油与硝酸在浓硫酸的作用下可得硝化甘油,过程中的反应方程式为4NH3+5O2
4NO+6H2O、O2+2NO=2NO2、3NO2+H2O═2HNO3+NO、 、
、 ,
,
故答案为:4NH3+5O2
4NO+6H2O、O2+2NO=2NO2、3NO2+H2O═2HNO3+NO、 、
、 ;
;
| ||
| △ |
 、
、 ,
,故答案为:4NH3+5O2
| ||
| △ |
 、
、 ;
;
点评:本题考查了有机物的合成,答题时注意规范运用化学用语,将无机制备和有机合成相结合,中等难度,灵活运用基础知识是解题的关键.

练习册系列答案
相关题目
下列物质的变化过程中,化学键没有被破坏的是( )
| A、食盐溶解 | B、干冰升华 |
| C、氯化铵受热 | D、氯化钠熔融 |
下列反应,离子方程式正确的是( )
| A、C12与H2O反应:Cl2+2H2O=2H++Cl-+ClO- |
| B、向H2O中投入少量Na2O2固体:2H2O+2Na2O2=2Na++2OH-+O2↑ |
| C、NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
| D、过量CO2通入漂白粉溶液中CO2+H2O+ClO-=HCO3-+HClO |
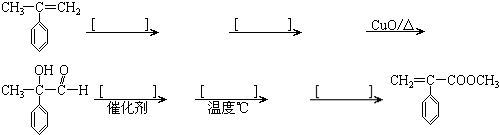

 代替化合物I发生反应②、反应③可以得到化合物VI(生产有机玻璃的中间体),化合物VI的结构简式为
代替化合物I发生反应②、反应③可以得到化合物VI(生产有机玻璃的中间体),化合物VI的结构简式为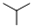 )在常温常压下为无色可燃性气体,微溶于水,可溶于乙醇、乙醚等,主要存在于天然气、炼厂气和裂解气中,经物理分离而获得,亦可由正丁烷经异构化制得.它主要用于与异丁烯反应制异辛烷,作为汽油辛烷值的改进剂,也可用作冷冻剂.
)在常温常压下为无色可燃性气体,微溶于水,可溶于乙醇、乙醚等,主要存在于天然气、炼厂气和裂解气中,经物理分离而获得,亦可由正丁烷经异构化制得.它主要用于与异丁烯反应制异辛烷,作为汽油辛烷值的改进剂,也可用作冷冻剂.
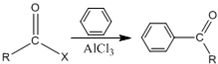 (X表示卤素;R表示烷基或氢原子)下面是一个以异丁烷为起始原料的有机合成路线:
(X表示卤素;R表示烷基或氢原子)下面是一个以异丁烷为起始原料的有机合成路线:
