题目内容
12.难溶电解质在水溶液中存在溶解平衡.请回答下列问题:(1)在2mL0.1mol/LMgCl2溶液中,加入4mL0.1mol/L的NaOH溶液,现象为生成白色沉淀,此反应的离子方程式为Mg2++2OH-=Mg(OH)2↓.将此混合液过滤,滤渣加入1mL0.1mol/L的FeCl3溶液,搅拌,现象为白色沉淀变为红褐色,反应的离子方程式为3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+.
(2)下列说法不正确的是CD.
A.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
B.对于Al(OH)3(s)?Al(OH)3(aq)?Al3++3OH-,前者为溶解平衡,后者为电离平衡
C.物质的溶解度随温度的升高而增加.故物质的溶解都是吸热的
D.除去溶液中的Mg2+,用OH-比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大.
分析 (1)MgCl2溶液中加入NaOH溶液,会生成白色的Mg(OH)2沉淀,据此书写离子方程式;向Mg(OH)2沉淀中加入FeCl3溶液,能发生沉淀的转化;
(2)A、为使离子完全沉淀,加入过量的沉淀剂,能使离子沉淀完全;
B、氢氧化铝是难溶物质,存在沉淀溶解平衡和电离平衡;
C、物质的溶解度不一定随温度的升高而增大;
D、Mg(OH)2的溶解度比MgCO3小.
解答 解:(1)MgCl2溶液中加入NaOH溶液,会生成白色的Mg(OH)2沉淀,离子方程式为:Mg2++2OH-=Mg(OH)2↓;
向Mg(OH)2沉淀中加入FeCl3溶液,能发生沉淀的转化,由白色的Mg(OH)2沉淀转化为红褐色的Fe(OH)3沉淀,离子方程式为:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+;
故答案为:生成白色沉淀;Mg2++2OH-=Mg(OH)2↓;白色沉淀变为红褐色;3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+;
(2)A、为使离子完全沉淀,加入过量的沉淀剂,能使离子沉淀完全,故A正确;
B、氢氧化铝是难溶物质,存在沉淀溶解平衡和电离平衡,故B正确;
C、物质的溶解度不一定随温度的升高而增大,如氢氧化钙溶液随温度的升高溶解度减小,故D错误;
D、除去溶液中的Mg2+,用OH-比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3小,故D错误;
故选CD.
点评 本题考查较为综合,涉及沉淀溶解平衡的计算应用,难溶物质的溶解度比较方法,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.表为短周期元素的一部分,请参照元素①~⑧在表中的位置,回答下列问题.
(1)元素⑦在元素周期表位置是第三周期ⅣA族.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式).HNO3>H2CO3>H2SiO3或(H4SiO4)
(3)④、⑤、⑥的离子半径由大到小的顺序为(填元素符号)O2->Na+>Al3+.
(4)由①和④组成的元素质重比为1:8的化合物的电子式是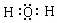 .
.
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为.2H2O+2Al+2OH-=2AlO2-+3H2↑.
| ① | ||||||
| ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式).HNO3>H2CO3>H2SiO3或(H4SiO4)
(3)④、⑤、⑥的离子半径由大到小的顺序为(填元素符号)O2->Na+>Al3+.
(4)由①和④组成的元素质重比为1:8的化合物的电子式是
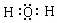 .
.(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为.2H2O+2Al+2OH-=2AlO2-+3H2↑.
11.下列分散系能产生“丁达尔效应”的是( )
| A. | 稀硫酸 | B. | 硫酸铜溶液 | C. | 氢氧化铁胶体 | D. | 酒精溶液 |
8.“分子马达”的关键组件三蝶烯的结构如图所示.下列说法正确的是( )
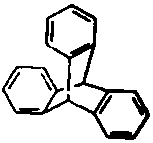

| A. | 三蝶烯是苯的同系物 | |
| B. | 三蝶烯能发生取代反应 | |
| C. | 三蝶烯的一氯代物有6种 | |
| D. | 三蝶烯分子中所有原子可能在同一平面上 |
1.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 250mL2mol•L-1的氨水中含有NH3•H2O的分子数为0.5NA | |
| B. | 0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.2 NA | |
| C. | 1 L 0.5 mol•L-1 Na2CO3溶液中含有的CO32-数为0.5NA | |
| D. | t℃时,pH=6 的纯水中含有OH-的个数为10-6NA |

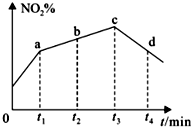 研究氧化物与悬浮在大气中的海盐粒子的相互作用时,涉及如下反应:
研究氧化物与悬浮在大气中的海盐粒子的相互作用时,涉及如下反应: