题目内容
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A、常温常压下,17g-14CH3所含的中子数为9NA |
| B、39g钾发生氧化还原反应时,一定失去NA个电子 |
| C、标准状况时,22.4L二氯甲烷所含有的分子数为NA |
| D、常温常压下,1mol氦气含有的核外电子数为 4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、该甲基中含有8个中子,17g该甲基的物质的量为1mol,含有8mol中子;
B、单质钾发生氧化还原反应后,一定变为+1价;
C、标况下,二氯甲烷为液态;
D、氦气是单原子分子,原子序数为2;
B、单质钾发生氧化还原反应后,一定变为+1价;
C、标况下,二氯甲烷为液态;
D、氦气是单原子分子,原子序数为2;
解答:
解:A、常温常压下,17g甲基(-14CH3)的物质的量为1mol,1mol该甲基中含有8mol中子,所含的中子数为8NA,故A错误;
B、单质钾发生氧化还原反应后,一定变为+1价,故39g钾即1mol钾发生氧化还原反应时,一定失1mol电子,个数为NA个,故B正确;
C、标况下,二氯甲烷为液态,故C错误;
D、氦气是单原子分子,原子序数为2,故常温常压下,1mol氦气含有的核外电子数为2NA,故D错误;
故选B.
B、单质钾发生氧化还原反应后,一定变为+1价,故39g钾即1mol钾发生氧化还原反应时,一定失1mol电子,个数为NA个,故B正确;
C、标况下,二氯甲烷为液态,故C错误;
D、氦气是单原子分子,原子序数为2,故常温常压下,1mol氦气含有的核外电子数为2NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
下列仪器:①烧杯;②蒸发皿;③表面皿;④烧瓶;⑤坩埚;⑥容量瓶;⑦量筒.能用酒精灯加热的是( )
| A、①②④⑤ | B、①③④⑤ |
| C、②③⑤⑥ | D、②③⑥⑦ |
下列物质加入水中,使水温显著降低的是( )
| A、固体氢氧化钠 | B、生石灰 |
| C、无水乙醇 | D、固体硝酸铵 |
铝、铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低.已知反应:BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是( )
| A、Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO |
| B、BeCl2溶液的pH>7,将其蒸干并灼烧后得到的残留物可能是BeCl2 |
| C、Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D、BeCl2水溶液的导电性强,故BeCl2是离子化合物 |
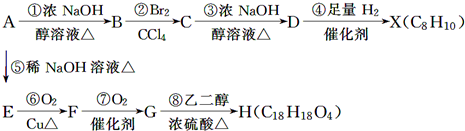
 (主要产物),1mol某芳香烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下面所示的一系列变化.
(主要产物),1mol某芳香烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如下面所示的一系列变化.