题目内容
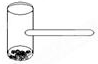 实验室里常用“碘锤”的玻璃仪器做碘的升华实验,该仪器为两头密封的玻璃窗,中间带有一根玻璃短柄.用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点.用此仪器不能反复进行的实验是( )
实验室里常用“碘锤”的玻璃仪器做碘的升华实验,该仪器为两头密封的玻璃窗,中间带有一根玻璃短柄.用此仪器进行有关实验时,具有装置简单、操作方便、现象明显、可反复使用等优点.用此仪器不能反复进行的实验是( )| A、NH4Cl受热分解的实验 |
| B、无水CuSO4与胆矾的互变实验 |
| C、白磷和红磷(已经抽出O2)在一定温度下相互转变的实验 |
| D、KMnO4受热分解的实验 |
考点:实验装置综合,同素异形体,铵盐
专题:实验设计题,元素及其化合物
分析:能在碘锤中发生反应,可说明在不同温度下发生不同的反应,加热时分解,冷却后可生成原物质,以此解答该题.
解答:
解:A.氯化铵受热分解生成氨气和氯化氢,冷却后氨气和氯化氢会反应生成氯化铵,重新凝结为固体,可以利用此装置进行反复实验,故A不选;
B.胆矾受热分解生成无水硫酸铜,硫酸铜和水结合重新生成结晶水合物,固体颜色发生变化,蓝色变化为白色,白色结合水生成蓝色晶体,能反复进行实验,故B不选;
C.红磷和白磷在不同的温度下可相互转化,能反复进行实验,故C不选;
D.高锰酸钾受热分解生成锰酸钾,二氧化锰和氧气,生成产物不能重新生成高锰酸钾,不能反复进行实验,故D选.
故选D.
B.胆矾受热分解生成无水硫酸铜,硫酸铜和水结合重新生成结晶水合物,固体颜色发生变化,蓝色变化为白色,白色结合水生成蓝色晶体,能反复进行实验,故B不选;
C.红磷和白磷在不同的温度下可相互转化,能反复进行实验,故C不选;
D.高锰酸钾受热分解生成锰酸钾,二氧化锰和氧气,生成产物不能重新生成高锰酸钾,不能反复进行实验,故D选.
故选D.
点评:本题综合考查元素化合物知识,为高频考点,侧重于反应的特征分析应用,注意把握装置的应用条件,题目难度中等.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列说法正确的是( )
| A、提纯鸡蛋白中的蛋白质时,可向鸡蛋清溶液中加入浓硫酸铵溶液,然后将所得沉淀滤出,经洗涤即得到较纯净的蛋白质 |
| B、油脂都不能使溴的四氯化碳溶液褪色 |
| C、石油分馏、煤的干馏均为物理变化 |
| D、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |

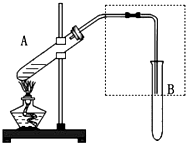 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置. 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究.回答下列问题: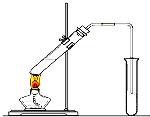 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: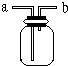 如图所示是中学化学实验中常见的装置,它有多种用途.
如图所示是中学化学实验中常见的装置,它有多种用途.