题目内容
A、B、C为短周期元素,在周期表中位置如图所示,A、C两元素原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
(1)写出A、B、C三种元素的名称 、 、 .
(2)B位于周期表中第 周期 族
(3)B离子结构示意图 .
| A | C | |
| B |
(2)B位于周期表中第
(3)B离子结构示意图
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:A、B、C为短周期元素,根据元素在周期表中位置知,A和C位于第二周期、B位于第三周期,设B原子序数为x,则A原子序数为x-9、C原子序数为x-7,A、C两元素的原子核外电子数之和等于B原子的质子数,则x-9+x-7=x,解得x=16,所以B是S元素,则A是N元素、C是F元素,再结合原子结构分析解答.
解答:
解:A、B、C为短周期元素,根据元素在周期表中位置知,A和C位于第二周期、B位于第三周期,设B原子序数为x,则A原子序数为x-9、C原子序数为x-7,A、C两元素的原子核外电子数之和等于B原子的质子数,则x-9+x-7=x,解得x=16,所以B是S元素,则A是N元素、C是F元素,
(1)通过以上分析知,A、B、C分别是氮、硫、氟元素,故答案为:氮;硫;氟;
(2)B是S元素,S原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故答案为:三;ⅥA;
(3)S2-离子核外有3个电子层,各层电子数为2、8、8,离子结构示意图为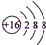 ,故答案为:
,故答案为: .
.
(1)通过以上分析知,A、B、C分别是氮、硫、氟元素,故答案为:氮;硫;氟;
(2)B是S元素,S原子核外有3个电子层、最外层电子数是6,所以S元素位于第三周期第VIA族,故答案为:三;ⅥA;
(3)S2-离子核外有3个电子层,各层电子数为2、8、8,离子结构示意图为
 ,故答案为:
,故答案为: .
.
点评:本题考查位置结构性质关系的综合应用,难度不大,注意根据同主族元素原子序数关系推断元素的种类.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
下列条件中,两种气体所含原子数一定相等的是( )
| A、同质量、不同密度的N2和CO |
| B、同温度、同体积的H2和N2 |
| C、同体积、同密度的C2H6和NO |
| D、同压强、同电子数的N2O和CO2 |
在电解水时,为了增强导电性,加入的电解质最好选用( )
| A、HCl |
| B、CuCl2 |
| C、Na2SO4 |
| D、CuSO4 |
已知A、B为单质,C为化合物.能实现上述转化关系的是( )
A+B
C
A+B
①符合上述转化关系的C溶于水不可能得到强碱溶液
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若A为光亮红色金属,则B可能为S
④若C的溶液中滴加铁氰化钾溶液有蓝色沉淀生成,则B可能为Cl2.
A+B
| 点燃 |
| 溶于水 |
| 惰性电极电解 |
①符合上述转化关系的C溶于水不可能得到强碱溶液
②若C的溶液遇Na2CO3,放出CO2气体,则A可能是H2
③若A为光亮红色金属,则B可能为S
④若C的溶液中滴加铁氰化钾溶液有蓝色沉淀生成,则B可能为Cl2.
| A、①②④ | B、②④ |
| C、①②③ | D、①② |
在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)?cC(g)+dD(g) 达到平衡后,测得C气体的浓度为0.5mol/L.当在恒温下,将密闭容器的体积缩小为
,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
| 1 |
| 2 |
| A、反应速率降低 |
| B、平衡向右移动 |
| C、B的转化率提高 |
| D、a+b<c+d |
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)→CO2(g)+3H2(g)-49.0kJ
②CH3OH(g)+1/2O2(g)→CO2(g)+2H2(g)+192.9kJ
下列说法正确的是( )
| A、1molCH3OH完全燃烧放出热量192.9 kJ |
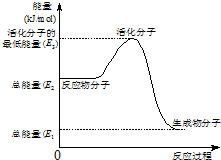
| B、②中的能量变化如图所示,则Q=E3-E1 |
| C、H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收热量 |
| D、根据②推知:在25℃,101 kPa时,1 molCH3OH(g)完全燃烧生成CO2和H2O放出的热量应大于192.9 kJ |