题目内容
18. 由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.
由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.(1)对该配合物的组成和结构分析如下:
①中心离子的价电子排布图为
 ,未成对电子数为5.
,未成对电子数为5.②不存在的作用力是be(填标号).
a.离子键 b.金属键 c.配位键 d.极性共价键 e.分子间作用力
③三种非金属元素的第一电离能从小到大的顺序为C<O<N,由其中两种元素组合可构成原子个数比为1:3的常见微粒,则该微粒的空间构型为平面三角形.
④与CN -互为等电子体的单质的结构式为N≡N,该单质中原子的杂化方式为sp.
(2)镍与铁同族.镍粉在CO气流中轻微加热,生成无色挥发性液态物质Ni(CO)4,推测Ni(CO)4的晶体类型为分子晶体.已知构成该晶体微粒的空间构型为正四面体,则Ni(CO)4易溶于bc(填标号)中.
a.水 b.四氯化碳 c.苯 d.硫酸镍溶液
(3)NaCl的晶胞结构示意图如图,NaCN的晶胞结构与其相似.已知NaCN晶体的密度为ρ g.cm-3,阿伏加德罗常数为NA,求晶胞边长a=$\root{3}{\frac{196}{ρ{N}_{A}}}$ cm.
分析 (1)①配合物Na2[Fe(CN)5(NO)]的中心离子为铁离子,铁离子的价层电子排布为3d5;
②配合物Na2[Fe(CN)5(NO)]中内界与外界之间是离子键,配体与中心离子间是配位键,配体内部碳氮之间及氮氧之间是极性共价键;
③同一周期元素的第一电离能随着原子序数的增大而呈增大趋势,氮元素原子2p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的;
由C、N、O中两种元素组合可构成原子个数比为1:3的常见微粒为NO3-;
④CN-含有2个原子、价电子总数为10,与CN-互为等电子体的单质为N2,N2分子中N原子形成一个σ键、含有1对孤对电子,杂化轨道数为2;
(2)Ni(CO)4为无色挥发性液态物质,熔沸点低,属于分子晶体;根据相似相溶原理分析溶解性;
(3)根据NaCl的晶胞结构可知,每个晶胞中含有4个钠离子和4个氯离子,所以NaCN的晶胞也含有4个钠离子和4个氰根离子,表示出晶胞质量,结合m=ρV计算晶胞的体积,进而计算晶胞的边长.
解答 解:(1)①配合物Na2[Fe(CN)5(NO)]的中心离子为铁离子,铁离子的价层电子排布为3d5,价电子排布图为 ,有5个未成对的电子,
,有5个未成对的电子,
故答案为: ;5;
;5;
②配合物Na2[Fe(CN)5(NO)]中内界与外界之间是离子键,配体与中心离子间是配位键,配体内部碳氮之间及氮氧之间是极性共价键,不存在的是金属键和分子间作用力,
故选:be;
③同一周期元素的第一电离能随着原子序数的增大而呈增大趋势,氮元素原子2p轨道为半满稳定状态,能量较低,第一电离能高于同周期相邻元素的,所以其第一电离能大小顺序是C<O<N,
由C、N、O中两种元素组合可构成原子个数比为1:3的常见微粒为NO3-,N原子孤电子对数为$\frac{5+1-2×3}{2}$=0,价层电子对数为3+0=3,故空间构型为平面三角形,
故答案为:C<O<N;平面三角形;
④CN-含有2个原子、价电子总数为10,与CN-互为等电子体的单质为N2,N2的结构式为N≡N,N2分子中N原子形成一个σ键、含有1对孤对电子,杂化轨道数为2,所以杂化方式为sp杂化,
故答案为:N≡N;sp;
(2)Ni(CO)4为无色挥发性液态物质,熔沸点低,属于分子晶体,呈正四面体构型,是对称结构,所以是非极性物质,根据相似相溶原理知,Ni(CO)4 易溶于非极性溶剂,苯、四氯化碳是非极性物质,所以Ni(CO)4 易溶于苯、四氯化碳,故选bc,
故答案为:分子晶体;bc;
(3)根据NaCl的晶胞结构可知,每个晶胞中含有4个钠离子和4个氯离子,所以NaCN的晶胞也含有4个钠离子和4个氰根离子,则晶胞质量为$\frac{4×49}{{N}_{A}}$g,晶体的密度为ρ g.cm-3,晶胞的体积为$\frac{4×49}{{N}_{A}}$g÷ρ g.cm-3=$\frac{196}{ρ{N}_{A}}$cm3,所以晶胞的边长为$\root{3}{\frac{196}{ρ{N}_{A}}}$cm,
故答案为:$\root{3}{\frac{196}{ρ{N}_{A}}}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、空间构型与杂化发生判断、电离能、等电子体、化学键、晶体类型与性质、晶胞的计算等知识点,注意同周期主族元素中第一电离能异常情况.

| A. | CH3CH2CH2CH2CH2Cl | B. | CH3CH2CHClCH2CH3 | ||
| C. | 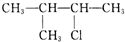 | D. | 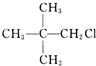 |
| A. | 将少量氯化钴晶体溶于一定浓度的盐酸溶液呈紫色,加热后溶液颜色变成蓝色 | |
| B. | 中和热测定实验中,环形玻璃搅拌棒不能用铜质搅拌棒代替 | |
| C. | 容量瓶、分液漏斗、滴定管使用时都必须检查是否漏水 | |
| D. | 滴定管水洗后必须烘干才能使用 |
| 元素 | H | Li | Be | B | C | N | O | F |
| 电负性 | 2.1 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 |
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.7 | 2.1 | 2.3 | 3.0 | 0.8 |
(1)预测周期表中电负性最大的元素应为F;估计钙元素的电负性的取值范围:0.8<X<1.2.
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是自上而下电负性降低;
简述元素电负性X的大小与元素金属性、非金属性之间的关系非金属性越强电负性越大,金属性越强电负性越小.
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为共价键,其理由是AlCl3中两电负性之差为1.5,Br元素的电负性小于Cl元素电负性,AlBr3中两电负性之差小于1.5.
①13Al3+ ②
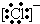 ③
③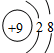 ④F- 其中核外电子数相同的是( )
④F- 其中核外电子数相同的是( )| A. | ①③ | B. | ②③④ | C. | ②④ | D. | ①③④ |
| A. | 苯酚不慎沾到皮肤上,要先用氢氧化钠溶液清洗,再用水洗 | |
| B. | 被蜜蜂或者蚂蚁蛰了以后痛痒难忍,可以用稀硼酸溶液清洗被蛰处,可减轻痛痒 | |
| C. | 浓硝酸不慎滴到皮肤上,皮肤变成黄色,是因为发生了颜色反应 | |
| D. | 甘油和乙二醇都可以用做抗冻剂,是因为这两个物质的凝固点比较低 |
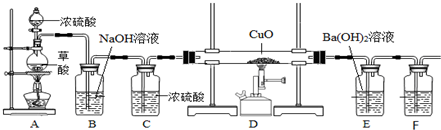
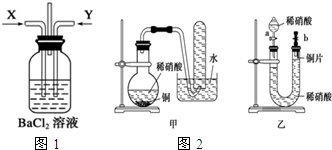 请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题.
请分析回答某同学在探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铜反应的实验中发生的有关问题.