题目内容
下列离子方程式正确的是( )
A、等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO
| ||||
| B、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | ||||
| C、1molCl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | ||||
| D、酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.等物质的量的碳酸氢钙与氢氧化钠反应生成碳酸钙和碳酸氢钠和水;
B.向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀,反应生成硫酸钡和偏铝酸钾、水;
C.碘离子的还原性强于二价铁离子,氯气应先氧化碘离子;
D.酸性条件下不能够生成氢氧根离子.
B.向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀,反应生成硫酸钡和偏铝酸钾、水;
C.碘离子的还原性强于二价铁离子,氯气应先氧化碘离子;
D.酸性条件下不能够生成氢氧根离子.
解答:
解:A.等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合,离子方程式:Ca2++HCO3-+0H-=CaCO3↓+H2O,故A错误;
B.向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀,离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故B正确;
C.1molCl2通入含1mol FeI2的溶液中,离子方程式:2I-+Cl2=2Cl-+I2,故C错误;
D.酸性条件下KIO3溶液与KI溶液发生反应生成I2,离子方程式:IO3-+5I-+6H+=3I2+3H2O,故D错误;
故选:B.
B.向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀,离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故B正确;
C.1molCl2通入含1mol FeI2的溶液中,离子方程式:2I-+Cl2=2Cl-+I2,故C错误;
D.酸性条件下KIO3溶液与KI溶液发生反应生成I2,离子方程式:IO3-+5I-+6H+=3I2+3H2O,故D错误;
故选:B.
点评:本题考查了离子方程式的书写,侧重考查反应物用量对反应的影响,题目难度较大,明确反应的实质是解题关键.

练习册系列答案
相关题目
配置480mL0.5mol/L的NaOH溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥480mL容量瓶、⑦药匙、⑧500mL容量瓶、⑨胶头滴管、⑩坩埚,必须要用到的仪器有( )
| A、①③④⑥⑦⑨ |
| B、①④⑦⑧⑨⑩ |
| C、①②④⑤⑧⑨ |
| D、①③④⑦⑧⑨ |
下列各组固体物质中,在加水或加热的条件下,都能放出CO2的是( )
| A、NaHCO3和Al2(SO4)3 |
| B、NaHCO3和Na2CO3 |
| C、MgSO4和CaCO3 |
| D、Na2CO3和Al(NO3)3 |
下列物质既能跟硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
| A、①②③④ | B、①和③ |
| C、③和④ | D、①和④ |
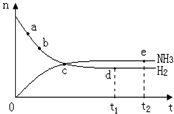 合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义,对密闭容器中的反应:N2(g)+3H2(g)
| 催化剂 |
| 高温高压 |
| A、点a的正反应速率比b点的大 |
| B、反应达到平衡时,v(N2)正=2v(NH3)逆 |
| C、点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D、其他条件不变,500℃下反应至t1时刻,n(H2)比图中d点值大 |
 如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).
如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出). )代替两个NH3与铂配位,则生成的产物
)代替两个NH3与铂配位,则生成的产物 和氯化钠溶液反应制取
和氯化钠溶液反应制取  的离子反应方程式
的离子反应方程式 )及呋喃(
)及呋喃( )形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式
)形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式