题目内容
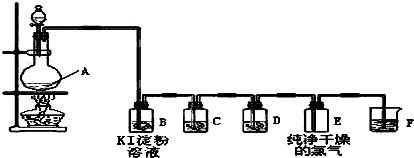
图为实验室制取和收集纯净干燥的氯气,并进行氯气的性质实验的装置图:
(1)反应前,在装置A中
(2)装置B中的现象是
(3)装置D中所装试剂是
(4)装置F中发生反应的化学方程式为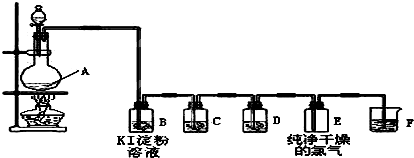
(1)反应前,在装置A中
分液漏斗
分液漏斗
装浓盐酸(填写仪器名称)圆底烧瓶
圆底烧瓶
装MnO2(填写仪器名称)装置A中反应的化学方程式为MnO2+4HCl
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl
MnCl2+Cl2↑+2H2O
.
| ||
(2)装置B中的现象是
溶液变蓝
溶液变蓝
反应的化学方程式为Cl2+2KI=2KCl+I2
Cl2+2KI=2KCl+I2
.(3)装置D中所装试剂是
浓硫酸
浓硫酸
,作用是吸收水分(干燥气体)
吸收水分(干燥气体)
.(4)装置F中发生反应的化学方程式为
Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
.
分析:(1)依据装置图和实验目的分析判断,制备氯气是用固体二氧化锰和液体浓盐酸,固体在圆底烧瓶中,盐酸在分液漏斗中;根据浓盐酸和二氧化锰的性质判断生成物,来书写反应方程式;
(2)氯气有氧化性,能置换出碘化钾中的碘,碘单质遇到淀粉变蓝;
(3)根据杂质的成分及性质分析;浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气;
(4)氯气和氢氧化钠反应,可以用氢氧化钠溶液吸收氯气,防止有毒气体污染空气.
(2)氯气有氧化性,能置换出碘化钾中的碘,碘单质遇到淀粉变蓝;
(3)根据杂质的成分及性质分析;浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气;
(4)氯气和氢氧化钠反应,可以用氢氧化钠溶液吸收氯气,防止有毒气体污染空气.
解答:解:(1)由装置图和实验目的分析判断,制备氯气是用固体二氧化锰和液体浓盐酸,固体在圆底烧瓶中,盐酸在分液漏斗中;浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原反应生成氯化锰、氯气和水,反应化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,
故答案为:分液漏斗;圆底烧瓶;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)氯气有氧化性,能置换出碘化钾中的碘,碘单质遇到淀粉变蓝;发生的化学方程式为:Cl2+2KI=2KCl+I2,
故答案为:溶液变蓝;Cl2+2KI=2KCl+I2;
(3)浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故答案为:浓硫酸;吸收水分(干燥气体);
(4)氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可用氢氧化钠溶液吸收多余的氯气,反应化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:2NaOH+Cl2 =NaCl+NaClO+H2O.
| ||
故答案为:分液漏斗;圆底烧瓶;MnO2+4HCl(浓)
| ||
(2)氯气有氧化性,能置换出碘化钾中的碘,碘单质遇到淀粉变蓝;发生的化学方程式为:Cl2+2KI=2KCl+I2,
故答案为:溶液变蓝;Cl2+2KI=2KCl+I2;
(3)浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气,故答案为:浓硫酸;吸收水分(干燥气体);
(4)氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可用氢氧化钠溶液吸收多余的氯气,反应化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:2NaOH+Cl2 =NaCl+NaClO+H2O.
点评:本题考查了氯气的实验室制备,氯气的化学性质的应用,主要是氯气的氧化性分析,收集纯净干燥的氯气的方法,题目较简单.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目