题目内容
请将下列五种物质:KBrO3、Br2、I2、KI、K2SO4分别填入下列对应的横线上,组成一个未配平的化学方程式:
(1) + +H2SO4→ + + +KBr+H2O;
(2)该反应中的氧化产物是 ,被还原的是 中(填写化学式)的 元素(填写元素符号);
(3)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□ +□ +□H2SO4→
(4)若转移电子总数为10mol,则反应中I2的物质的量为 .
(1)
(2)该反应中的氧化产物是
(3)请将反应物的化学式及配平后的系数填入下列相应的位置中:
□
(4)若转移电子总数为10mol,则反应中I2的物质的量为
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)根据Br元素反应后化合价降低可知,还需填入还原剂KI作反应物,其它物质为生成物;
(2)Br元素的化合价降低,I元素的化合价升高;
(3)根据(1)的分析结合电子、原子守恒分析解答;
(4)反应中KI→I2,I元素化合价由-1价升高为0价,氧化产物只有I2,根据电子注意守恒计算生成I2的物质的量.
(2)Br元素的化合价降低,I元素的化合价升高;
(3)根据(1)的分析结合电子、原子守恒分析解答;
(4)反应中KI→I2,I元素化合价由-1价升高为0价,氧化产物只有I2,根据电子注意守恒计算生成I2的物质的量.
解答:
解:(1)根据Br元素反应后化合价降低可知,还需填入还原剂KI作反应物,其它物质I2、Br2、K2SO4、KBr为生成物,该反应为KBrO3+KI+H2SO4→I2+Br2+K2SO4+KBr+H2O,
故答案为:KBrO3;KI;I2;Br2;K2SO4;
(2)KBrO3中Br元素的化合价降低,被还原,I元素的化合价升高,则被氧化,所以I2为氧化产物,故答案为:I2;KBrO3;Br;
(3)I元素的化合价由-1价升高为0,Br元素的化合价由+5价降低为0、-1价,由电子及原子守恒可知反应为3KBrO3+16KI+9H2SO4=8I2+Br2+9K2SO4+KBr+9H2O,
故答案为:3KBrO3;16KI;9;
(4)反应中KI→I2,I元素化合价由-1价升高为0价,氧化产物只有I2,故转移10mol电子生成I2的物质的量为
=5mol,故答案为:5mol.
故答案为:KBrO3;KI;I2;Br2;K2SO4;
(2)KBrO3中Br元素的化合价降低,被还原,I元素的化合价升高,则被氧化,所以I2为氧化产物,故答案为:I2;KBrO3;Br;
(3)I元素的化合价由-1价升高为0,Br元素的化合价由+5价降低为0、-1价,由电子及原子守恒可知反应为3KBrO3+16KI+9H2SO4=8I2+Br2+9K2SO4+KBr+9H2O,
故答案为:3KBrO3;16KI;9;
(4)反应中KI→I2,I元素化合价由-1价升高为0价,氧化产物只有I2,故转移10mol电子生成I2的物质的量为
| 10mol |
| 2 |
点评:本题考查氧化还原反应,为高频考点,把握反应中元素化合价变化为解答的关键,侧重氧化还原反应配平及守恒法应用的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
A、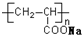 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| B、用于现代建筑的钢筋混凝土不属于复合材料 |
| C、pH=2的盐酸和NH4Cl溶液中,水电离出的c(H+)相等 |
| D、常温时铝遇浓硝酸钝化,是由于铝元素有很强的金属性 |
被蚊虫叮咬后.涂些含有碱性物质(如NH3?H2O)的药水,可减轻痛痒.NH3?H2O中的N元素的化合价为( )
| A、-3 | B、0 | C、+3 | D、+5 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、78g苯分子中含有的碳碳双键数为3NA |
| B、7.8g Na2O2含有的阴离子数目为0.2NA |
| C、12g石墨烯(也就是单层石墨)中含有六元环的个数为NA |
| D、常温常压下,2g D216O中含中子数、质子数、电子数均为NA |
将0.015mol Fe3O4完全溶于硫酸中,再加入K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转化为Fe3+,Cr2O72-全部还原为Cr3+,则K2Cr2O7溶液的物质的量浓度为( )
| A、0.05mol/L |
| B、0.1mol/L |
| C、0.2mol/L |
| D、0.3mol/L |
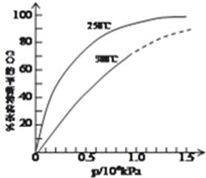 在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示.
在容积可变的密闭容器中,由CO和H2合成甲醇CO(g)+2H2(g)═CH3OH(g),CO在不同温度下的平衡转化率与压强的关系如图所示. 表示的分子式
表示的分子式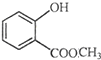 中含有的官能团的名称为
中含有的官能团的名称为