题目内容
20.如图是元素周期表的一部分,表中的每个字母代表一种短周期元素
请填写下列空白:
(1)A与C形成A2C的电子式为
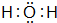 D 的原子结构示意图
D 的原子结构示意图 .
.(2)用一个化学方程式表示C的非金属性比E的非金属性强2H2S+O2=2S↓+2H2O.
分析 由短周期元素的位置可知,A为H元素,B为N元素,C为O元素,D为Al,E为S元素.
(1)H2O中氢原子与氧原子之间形成1对共用电子对;D为Al元素,原子核外有13个电子,有3个电子层,各层电子数为2、8、3;
(2)用单质之间相互置换可以证明元素非金属性强弱.
解答 解:由短周期元素的位置可知,A为H元素,B为N元素,C为O元素,D为Al,E为S元素.
(1)H2O中氢原子与氧原子之间形成1对共用电子对,电子式为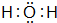 ;D为Al元素,原子核外有13个电子,有3个电子层,各层电子数为2、8、3,原子结构示意图为
;D为Al元素,原子核外有13个电子,有3个电子层,各层电子数为2、8、3,原子结构示意图为 ,
,
故答案为: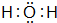 ;
; ;
;
(2)用单质之间相互置换可以证明元素非金属性强弱,反应方程式为:2H2S+O2=2S↓+2H2O,
故答案为:2H2S+O2=2S↓+2H2O.
点评 本题考查元素周期表与元素周期律,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
10.以下变化过程属于氧化还原反应的是( )
| A. | 灼烧氯化钠火焰呈黄色 | B. | 碘的升华 | ||
| C. | 明矾常用于净水 | D. | 常温下浓硫酸使铝钝化 |
11.将5.6g Cu、Mg合金投入到一定量的硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下混合气体VL(HNO3被还原为NO和NO2);若向反应后的溶液中加入足量氢氧化钠溶液,待金属元素全部沉淀后,再将沉淀过滤、洗净、干燥后称量质量为10.7g,则下列分析正确的是( )
| A. | 沉淀中氢氧根的质量为5.1g | B. | V为2.24L | ||
| C. | Cu的物质的量为0.1mol | D. | 反应后溶液呈中性 |
8.如图为元素周期表的一部分,下列有关B、W、X、Y、Z五种元素的叙述中正确的是( )
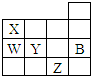

| A. | 常压下,五种元素的单质中,Z单质的沸点最高 | |
| B. | X的氢化物沸点比W的氢化物沸点高 | |
| C. | Y元素氧化物的水化物酸性比W的强 | |
| D. | Y、Z的简单阴离子的电子层结构都与B原子的相同 |
15.下列反应过程需要吸收热量的是( )
| A. | 燃烧 | B. | 浓硫酸溶于水 | C. | 酸碱中和 | D. | 水的电离 |
5.下列反应对应的离子方程式中正确的是( )
| A. | FeCl3溶液中加入铁粉:Fe+Fe3+═2Fe2+ | |
| B. | NH4HSO4溶液中加入少量NaOH:NH4++OH-═NH3•H2O | |
| C. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| D. | 氯气通入Na2SO3溶液中:Cl2+SO32-+H2O═SO42-+2H++2Cl- |
12.下列关于反应2Na2O2+2H2O═4NaOH+O2↑的说法正确的是( )
| A. | 过氧化钠是氧化剂,水是还原剂 | B. | Na2O2是还原剂,水是氧化剂 | ||
| C. | 过氧化钠既是氧化剂又是还原剂 | D. | 水既是氧化剂又是还原剂 |
9.下列实验或操作合理的是( )
| A. | 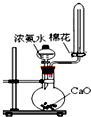 制氨气 | B. | 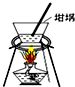 蒸发、浓缩、结晶 | ||
| C. | 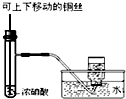 制备并收集少了二氧化氮 | D. | 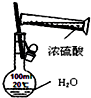 浓硫酸稀释 |
 .
.